2. LES ÉTUDES ÉPIDEMIOLOGIQUES SONT LA PRINCIPALE SOURCE DE QUANTIFICATION DU RISQUE (4 ( * ))
Limiter cette probabilité d'apparition suppose que l'on est capable de quantifier le risque radiologique. Parmi les effets biologiques des rayonnements ionisants, le plus important des effets à long terme est l'induction des cancers. On peut apprendre beaucoup sur la nature et les conditions de l'induction des cancers grâce à des expériences de laboratoire sur des systèmes cellulaires et des animaux. Néanmoins jusqu'ici la méthode la plus adaptée pour étudier les cancers radioinduits est l'étude épidémiologique des populations humaines.
2.1 Les études épidémiologiques sont d'un intérêt essentiel pour l'estimation quantitative des effets des rayonnements ionisants
Dans son acceptation la plus large l'épidémiologie est une discipline scientifique qui a pour objet l'étude des problèmes de santé dans les populations. Elle est au sens de l'OMS cette branche de la science médicale qui s'occupe de l'étude des facteurs de milieu, des facteurs individuels et autres qui influent de quelque manière sur la santé humaine. Le concept d'épidémiologie (comme d'ailleurs celui d'épidémie) a donc largement dépassé une acceptation initiale limitée aux seules maladies infectieuses. En ce sens les effets sanitaires des rayonnements ionisants entrent tout à fait dans le cadre de l'épidémiologie.
2.1.1 Qu'est-ce qu'une étude épidémiologique ?
L'épidémiologie a traditionnellement trois objectifs : elle peut tout d'abord chercher à décrire les phénomènes sanitaires apparaissant au sein d'une population déterminée (fréquence, répartition géographique, évolution temporelle...) ; elle peut également chercher à préciser qualitativement et quantitativement les causes d'apparition, d'aggravation ou d'atténuation de la fréquence des pathologies ; enfin elle peut être utilisée pour évaluer l'efficacité des interventions publiques visant à améliorer la santé des populations. L'étude des effets des rayonnements ionisants relève de la deuxième catégorie.
L'épidémiologie est essentiellement une science d'observation : les études sont gouvernées par les circonstances plutôt que par la volonté du chercheur, à qui échappent la maîtrise des conditions d'exposition, le « contour » de la population étudiée, la distribution des doses au sein de cette population... Dans le cas des rayonnements ionisants, les expositions résultent par exemple :
- de la localisation géographique de l'individu exposé (bombardements d'Hiroshima et Nagasaki) ;
- de la proximité de la résidence avec des sources d'exposition (exposition au rayonnement terrestre, exposition au radon dans les maisons) ;
- de la profession (peintres en cadrans lumineux, mineurs d'uranium, travailleurs de l'industrie nucléaire...) ;
- du traitement de certaines maladies (spondylarthrite ankylosante, cancer de l'utérus...) ; etc.
Il en découle que les effets intéressant le chercheur ne peuvent pas nécessairement être étudiés directement ou avec la précision voulue, que certaines procédures tendant à limiter les biais méthodologiques ne peuvent pas être mises en oeuvre, enfin que les études ne peuvent pas être répétées au gré du chercheur.
Nous ne sommes pas égaux devant le risque de maladie. Chacun peut constater qu'il existe des différences de sensibilité entre individus ou sous-groupes dans une population donnée. L'étude épidémiologique a pour but d'identifier l'existence et l'influence des facteurs de différenciation vis-à-vis du risque de maladie, appelés " facteurs de risque". Le problème fondamental de l'épidémiologie est d'interpréter l'éventuelle association statistique entre le facteur de risque et la maladie étudiés afin de conclure sur l'existence d'une relation de causalité entre ce facteur de risque et la maladie.
Je laisse ici la parole au Pr. Marcel GOLDBERG et à Mme Elisabeth CARDIS (5 ( * )) qui montrent avec clarté comment ne pas confondre association statistique et causalité.
"En premier lieu, il ne faut pas oublier qu'une association statistique peut être fallacieuse, c'est-à-dire due à un biais, à une erreur quelconque ou au hasard. Ainsi il est pas rare, par exemple, de constater que, pour une même pathologie, le pronostic est nettement plus défavorable pour les patients soignés en milieu hospitalier spécialisé que pour ceux traités en ville ; mais l'explication de la liaison observée entre évolution de la maladie et type de prise en charge médicale réside dans le fait que ce sont les malades initialement les plus gravement atteints qui vont à l'hôpital, alors que les cas bénins sont soignés par leur médecin traitant habituel."
"Un autre type d'erreur consiste à interpréter une association « à l'envers » . Ainsi, si l'on observe que les fumeurs ont fréquemment l'index jaune, l'erreur consisterait à interpréter cette association dans le sens : index jaune ? fumeur, alors que c'est parce que ces sujets sont plus souvent fumeurs qu'ils ont plus fréquemment l'index jaune. Cet exemple est caricatural mais il existe de nombreuses situations où le sens de la relation entre maladie et facteur de risque n `est pas aussi évident (par exemple, si on étudie le rôle iatrogène (6 ( * )) de certains médicaments : a-t-on eu telle maladie à la suite de la prise de ce médicament ? ou au contraire a-t-on commencé à prendre ce médicament parce qu'on avait déjà les premiers signes de cette maladie ?)."
"Un autre type d'association est l'association indirecte. Dans un tel cas, une variable est liée à l'événement étudié, mais en fait ne joue un rôle que par l'intermédiaire d'une autre variable. Un exemple classique est celui de l'obésité et des cardiopathies ischémiques. Il existe une association forte entre obésité et incidence de la maladie ; en fait cette association s'explique par le fait que l'obésité entraîne une augmentation de la pression artérielle : c'est l'hypertension qui est la cause de l'augmentation du risque, alors que l'obésité isolée ne modifie pas celui-ci. On peut schématiser cette association indirecte de la façon suivante : obésité ? hypertension ? maladie."
"Un cas particulier de l'association indirecte est celle qui est due à un facteur de confusion. Ce type d'association est particulièrement fréquent en épidémiologie. Il se produit dans les circonstances suivantes. On observe une liaison entre un facteur dont on étudie le rôle et une maladie ; par ailleurs, il existe un autre facteur, le facteur de confusion, lui-même lié à la fois au facteur étudié et à la maladie. La présence du facteur de confusion peut produire l'association observée initialement, même si le facteur dont on étudie le rôle et la maladie sont indépendants, selon le schéma :"
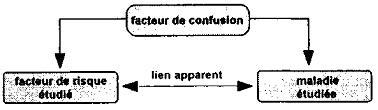
Un aspect important de l'étude épidémiologique consiste donc à détecter l'existence puis éliminer l'influence de ces facteurs de confusion. Cela est facile pour des déterminants simples comme l'âge, le sexe et l'appartenance ethnique. Cela nécessite de bonnes « archives » ou des entretiens avec les individus étudiés pour la plupart des autres facteurs (histoire professionnelle, consommation de tabac, habitudes alimentaires...).
C'est l'élimination correcte de ces éventuels facteurs de confusion qui permet de réfuter ou de mettre en évidence de façon qualitative, et si possible quantitative, le lien causal entre le facteur de risque et l'effet étudié (maladie).
2.1.2 Les deux méthodes de base de l'épidémiologie
L'enquête de cohorte est le premier grand type d'étude épidémiologique. Elle s'appuie sur la constitution d'une cohorte d'individus indemnes vis-à-vis de la maladie étudiée, suivie sur une période déterminée. Les caractéristiques pertinentes relatives aux individus sont relevées au début de l'enquête, en particulier le degré d'exposition au facteur de risque étudié. Pendant la durée de l'enquête l'observateur collecte l'information relative aux décès (ou à l'incidence de la maladie). Les conclusions sont tirées à l'extinction de la cohorte. En fait dans la plupart des cas le début de la période d'observation est antérieur, voire très antérieur, au lancement de l'enquête (études rétrospectives). Il faut donc reconstituer a posteriori l'exposition des individus au facteur de risque, leurs caractéristiques personnelles ainsi que l'incidence de la maladie ou la cause de décès ; ceci n'est pas toujours facile.
Le principal avantage des enquêtes de cohorte est qu'elles permettent de réunir, dans de bonnes conditions, les informations nécessaires au calcul du risque. Leurs principaux inconvénients sont liés à la longueur nécessaire du suivi : pour une étude « contemporaine » portant sur une cohorte encore en vie, il faut attendre le décès de ensemble des membres de la cohorte ; pour une étude « historique » ou rétrospective il faut s'appuyer sur des données tirées du passé, qui n'ont pas toujours le degré de fiabilité nécessaire. Ces enquêtes sont ainsi pénalisées par une lenteur, une lourdeur, donc un coût assez élevés.
L'autre grand type d'étude épidémiologique est l'enquête cas-témoin. On sélectionne là un groupe de sujets atteints de la maladie étudiée : les cas (ils sont supposés représentatifs de l'ensemble des personnes souffrant de cette pathologie, pour ce qui est de l'exposition au facteur de risque étudié) ; on sélectionne par ailleurs un ou plusieurs groupes de sujets indemnes : les témoins. L'inférence de la maladie est fondée sur la comparaison entre le niveau des différents facteurs de risque étudiés entre les cas et les témoins.
Les avantages de l'étude cas-témoin viennent en contrepoint des inconvénients de l'étude de cohorte : la première est rapide car l'événement recherché - la maladie - est déjà survenu au lancement de l'enquête ; elle est peu coûteuse car la taille des groupes observés n'est en général pas très élevée ; enfin le contexte de travail est souvent plus commode (les témoins sont fréquemment sélectionnés en milieu hospitalier). En revanche les inconvénients tiennent à l'obligation de reconstituer a posteriori toutes les « données » (qui n'en sont donc pas, au sens strict...) ce qui peut introduire un biais (volontaire ou involontaire) tant de la part de l'enquêteur que de la personne répondant à ses questions. Pour cette raison l'enquête cas-témoin est généralement moins fiable que l'enquête de cohorte. Il faut noter au demeurant que l'on peut inclure des enquêtes cas-témoins à l'intérieur d'une enquête cohorte si l'on cherche à cerner un aspect particulier du risque subi par la cohorte.
2.1.3 Quelques questions d'importance pour la qualité des études épidémiologiques
J'ai déjà mentionné la nécessité d'identifier et d'éliminer les facteurs de confusion. Il existe d'autres paramètres importants à prendre en compte pour conduire une étude épidémiologique réellement informative.
1. La qualité des données recueillies (ou reconstituées) est indispensable. Il est impensable d'effectuer un bon traitement statistique d'une part, une interprétation pertinente d'autre part si les données de départ sont floues, mal définies ou de façon générale peu propices à l'investigation. Cette nécessaire exigence concerne donc :
- la qualité du suivi, dans le cas des études cohortes : l'exhaustivité est souhaitable, l'idéal étant l'extinction complète de la cohorte étudiée ;
- la qualité dans la méthode de détection des effets : par exemple il n'est pas rare que la surveillance exercée au regard de la maladie étudiée soit plus importante chez les individus exposés que dans le groupe non exposé qui sert de référence ;
- la qualité dans le relevé de l'exposition au facteur de risque : par exemple, dans les premières études sur l'irradiation in utero il est désormais clair que les parents des enfants « cas » (donc malades) ont été plus portés à signaler une irradiation prénatale aux rayons X que les parents des enfants « témoins » (donc sains) ;
- la qualité des informations enregistrées : a/ dans le domaine de l'effet étudié, il faut par exemple un relevé correct des causes de décès (ou de l'incidence de la maladie) : il n'est pas rare que la cause réelle de la mort indiquée sur les registres soit fausse, ce qui peut conduire à une incertitude allant jusqu'à 10 % ; b/ dans le domaine du facteur de risque étudié, la qualité de l'information dosimétrique est essentielle (pour ce qui est des études portant sur les effets des rayonnements ionisants) ;
2. De même il particulièrement important que les groupes exposés et non exposés soient réellement comparables. Le phénomène connu sous le nom de healthy worker effect, ou effet du travailleur sain, en est l'illustration la plus frappante. Il a d'ailleurs donné lieu à quelques échanges lors de l'audition du 23 novembre dernier. Rappelons que l'effet du travailleur sain se manifeste par un taux général de mortalité et des taux de morbidité moindres chez les travailleurs que dans la population générale. La cause généralement alléguée est l'application de critères de sélection sanitaire à l'embauche.
La conséquence sur la pertinence d'études épidémiologiques conduites sur les travailleurs est, si l'on n'y prend garde, une sous-estimation du risque réel. Cette sous-estimation est susceptible d'apparaître si l'on compare un groupe exposé constitué de travailleurs à un groupe non exposé constitué de personnes de la population générale. En revanche l'effet du travailleur sain est éliminé si le groupe de référence (non exposé) est constitué lui aussi de travailleurs, ce qui est généralement le cas.
3. Enfin l'étude épidémiologique doit s'appuyer sur des méthodes d'analyse solides. En particulier il doit y avoir une bonne adéquation entre les phénomènes étudiés, les données recueillies et les modèles d'interprétation utilisés. Cela commence par une définition rigoureuse du risque étudié, j'entends par là non seulement la précision sémantique dans la caractérisation du risque mais aussi une formulation mathématique pertinente et adaptée.
Il est relativement aisé de cerner la notion qualitative du risque, à savoir l'induction d'un cancer. En revanche il est plus difficile de trouver un indicateur numérique permettant de mesurer les niveaux de risque et de déterminer la ou les loi(s) d'induction des cancers par rayonnements, et ayant une pertinence universelle :
- trois notions sont aisément accessibles à l'entendement : le risque absolu, égal au nombre de cas observés ; l' excès de risque absolu, égal à la différence entre le nombre de cas observés et le nombre de cas attendus ; l' excès de risque relatif, qui rapporte le précédent à une base de référence constituée par le nombre de cas attendus ;
- afin de comparer les risques dus à des niveaux d'exposition différents, on peut rapporter l'indicateur précédent à la dose moyenne reçue par la population étudiée ; cela revient à définir un coefficient de risque relatif, dont le domaine de validité est limité à une gamme d'exposition où l'on peut constater une certaine proportionnalité entre l'effet (l'induction d'un cancer) et la cause (la dose de rayonnement) ;
- pour comparer des études différentes, il est souhaitable de diviser l'indicateur précédent par une grandeur mesurant le « volume » du suivi, à savoir le produit du nombre de personnes suivies par le nombre d'années pendant lequel elles ont été suivies (7 ( * )) ;
- les grandeurs précédentes sont les indicateurs relativement « bruts » que l'on peut déterminer à partir des résultats de base issus de l'investigation épidémiologique ; ils en sont d'ailleurs, si je puis dire, le « langage » le plus direct ; pour une interprétation plus poussée de ces résultats, il est indispensable de construire des grandeurs plus complexes qui permettent de déterminer des estimations de « risque vie entière » ; il s'agit en l'occurrence 1/ de s'affranchir des différences entre les périodes de suivi dans les diverses études apportant l'information ; 2/ de reconnaître l'impact de facteurs socioculturels, environnementaux, ethniques, etc. sur le niveau de référence du risque (nombre de cas attendus) ; 3/ de prendre en compte, si nécessaire, l'effet du sexe et de l'âge à l'exposition ; ces contraintes laissent encore une relative liberté de choix à l'épidémiologiste puisque par exemple l'UNSCEAR d'un côté et le Comité ad hoc de l'Académie des Sciences américaine de l'autre côté ont choisi deux définitions différentes d'un risque vie entière ; la question est d'importance puisque c'est généralement à partir de ce genre d'estimateur du risque que sont dérivées les valeurs limites recommandées pour la radioprotection ;
- enfin aucun des indicateurs choisis par l'UNSCEAR ou l'Académie des Sciences américaine ne donne d'information sur l'époque à laquelle surviennent les cancers radioinduits ; il peut donc être nécessaire de compléter les estimations précédentes, qui ne s'intéressaient qu'à la probabilité du risque, par un autre indicateur qui reflète mieux le facteur temps ; on peut par exemple choisir de calculer la perte d'espérance de vie due aux cancers radioinduits.
Par ailleurs, il va de soi que les considérations précédentes peuvent s'appliquer soit au calcul du risque global de cancer chez un individu soit de façon différenciée aux cancers susceptibles d'apparaître dans les divers organes du corps humain.
Enfin, au delà de la définition du risque, l'épidémiologiste doit s'assurer de la pertinence des méthodes d'analyse qu'il met en oeuvre, que ce soit pour définir des sous-groupes au sein de la population étudiée, pour choisir un modèle de relation entre le niveau de dose et le niveau d'induction des cancers, ou pour établir comment transférer à une autre population les estimateurs de risques calculés sur la population étudiée... La route est longue des investigations sur le terrain à la publication dans les revues scientifiques internationales !
D'autant plus longue que les études directes des effets des faibles doses sont impuissantes à fournir des estimations de risque suffisamment précises pour être utilisables en matière de politique de radioprotection.
* 4 La plupart des développements présents ici sont tirés soit des rapports de l'UNSCKAR (Comité scientifique des Nations Unies sur les Effets des Rayonnements atomiques) soit d'un article de M. GOLDBERG (INSERM, Unité 88) et Mme CARDIS (Centre international de Recherches sur le Cancer) paru dans la revue Radioprotection en 1994 (Vol 29, supplément au n° 3), soit d'entretien avec diverses personnalités
* 5 op. cit.
* 6 iatrogène qui est provoqué par le médecin
* 7 Car du point de vue de l'information apportée par l'enquête, il est équivalent de suivre 1000 personnes pendant 1 an et 100 personnes pendant 10 ans, par exemple.







