- AVANT-PROPOS
- QUELQUES DÉFINITIONS D'INTÉRÊT
GÉNÉRAL
- L'ESSENTIEL
- PREMIÈRE PARTIE
LES PERSPECTIVES PLEINES DE PROMESSES DE L'IA EN SANTÉ
- DEUXIÈME PARTIE
EFFICACITÉ ET ÉTHIQUE,
LES DEUX PILIERS DE L'ACCEPTABILITÉ
DE L'IA EN SANTÉ
- CONCLUSIONS ET RECOMMANDATIONS
- EXAMEN EN DÉLÉGATION
- LISTE DES PERSONNES ENTENDUES
N° 611
SÉNAT
SESSION ORDINAIRE DE 2023-2024
Enregistré à la Présidence du Sénat le 21 mai 2024
RAPPORT D'INFORMATION
FAIT
au nom de la délégation
sénatoriale à la prospective (1)
sur
« IA et
santé »,
Par M. Christian REDON-SARRAZY et Mme Anne VENTALON,
Sénateur et Sénatrice
(1) Cette délégation est composée de : Mme Christine Lavarde, présidente ; MM. Daniel Guéret, Jean-Raymond Hugonet, Mme Anne Ventalon, MM. Christian Redon-Sarrazy, Jean-Jacques Michau, Guislain Cambier, Mmes Annick Jacquemet, Nadège Havet, Cécile Cukierman, Vanina Paoli-Gagin, MM. Yannick Jadot, Bernard Fialaire, vice-présidents ; MM. Bruno Belin, Stéphane Sautarel, Rémi Cardon, secrétaires ; MM. Pierre Barros, Jean-Baptiste Blanc, François Bonneau, Christian Bruyen, Christophe Chaillou, Raphaël Daubet, Vincent Delahaye, Mmes Patricia Demas, Amel Gacquerre, MM. Roger Karoutchi, Khalifé Khalifé,Vincent Louault, Louis-Jean de Nicolaÿ, Alexandre Ouizille, Didier Rambaud, Mme Marie-Pierre Richer, MM. Pierre-Alain Roiron, Jean Sol, Mmes Sylvie Vermeillet, Mélanie Vogel.
AVANT-PROPOS
Christine Lavarde, présidente de la délégation à la prospective
À l'instar des révolutions technologiques générales que furent la machine à vapeur, l'électricité ou encore Internet, l'intelligence artificielle (IA) pourrait profondément changer la façon dont nous vivons et travaillons, et ceci dans tous les domaines. Pourtant, dans le secteur public, les expérimentations restent à ce jour limitées, les annonces modestes, et la parole très prudente.
Pour l'État, les collectivités territoriales et les autres acteurs publics, le potentiel de l'IA générative est immense. Bien utilisée, elle pourrait devenir un formidable outil de transformation de l'action publique, rendant celle-ci non seulement plus efficace - qu'il s'agisse de contrôle fiscal ou de diagnostic médical - mais aussi plus proche des citoyens, plus accessible, plus équitable, plus individualisée et finalement plus humaine - avec une capacité inédite à s'adapter aux spécificités de chaque élève, de chaque demandeur d'emploi, de chaque patient ou de chaque justiciable.
Pour autant, le secteur public n'est pas un secteur comme les autres. Si l'IA n'est qu'un outil, avec ses avantages, ses risques et ses limites, son utilisation au service de l'intérêt général ne pourra se faire qu'à condition que les agents, les usagers et les citoyens aient pleinement confiance.
La confiance, cela passe d'abord par la connaissance : par son approche sectorielle, la délégation espère contribuer à démystifier une technologie qui suscite encore beaucoup de fantasmes, et à en montrer concrètement les possibilités comme les limites.
La confiance, c'est aussi et surtout l'exigence : une IA au service de l'intérêt général, c'est une IA au service des humains (agents et usagers), et contrôlée par des humains (citoyens). C'est aussi une IA qui s'adapte à notre organisation administrative et à notre tradition juridique, et qui garantit le respect des droits et libertés de chacun. C'est, enfin, une IA qui n'implique ni dépendance technologique, ni renoncement démocratique.
QUELQUES DÉFINITIONS D'INTÉRÊT GÉNÉRAL
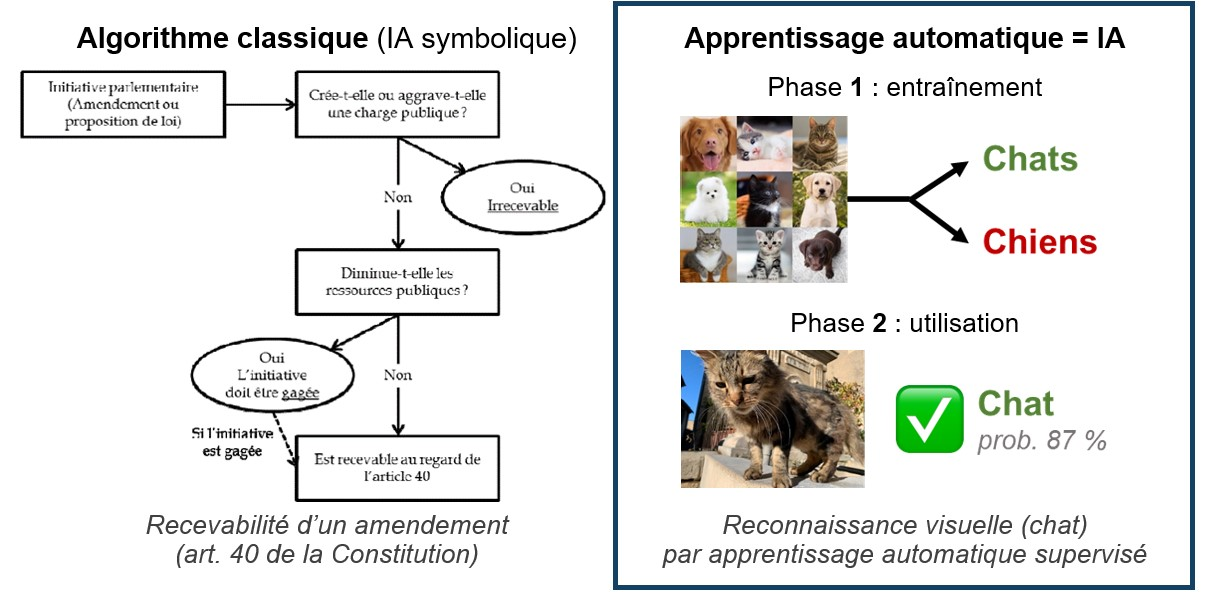
· Intelligence artificielle (IA) : terme apparu en 1956 qui, dans son sens actuel, désigne un programme informatique (algorithme) fondé sur l'apprentissage automatique, ou apprentissage machine (machine learning). Cette technique permet à la machine d'apprendre par elle-même à effectuer certaines tâches à partir d'un ensemble de données d'entraînement. Elle repose sur une approche statistique (IA connexionniste), par opposition à l'informatique « classique » (IA symbolique), qui consiste à suivre une suite de règles logiques préétablies (de type « SI... ET... ALORS... »).
· Apprentissage profond (deep learning) : perfectionnement de l'apprentissage automatique grâce à une organisation en réseaux de neurones artificiels, où chaque « neurone » est une fonction mathématique qui ajuste ses paramètres au fur et à mesure de l'entraînement.
Les progrès sont spectaculaires à partir des années 2010 du fait de 3 facteurs : la sophistication des modèles, la disponibilité des données, et surtout l'explosion de la puissance de calcul.
L'IA est désormais présente dans de très nombreuses applications de notre quotidien.
· IA générative : modèles d'IA comme ChatGPT spécialisés dans la création de contenus originaux et réalistes, en réponse à une instruction formulée en langage naturel (le prompt). Le contenu peut être du texte, mais aussi du code informatique, un fichier Excel, une image (Dall-E, Midjourney), un fichier audio ou vidéo (Sora), etc.
· Grands modèles de langage ou LLM (large language models) : modèles d'IA spécialisés dans le traitement du langage naturel, dans toutes les langues.
Entraînés sur d'immenses quantités de textes, ils établissent des relations mathématiques entre les mots et les notions sous-jacentes, à partir de calculs de probabilités.
Les IA génératives sont construites sur des LLM (ex. modèle GPT-4 pour ChatGPT).
Le lancement de ChatGPT, fin 2022, par la société OpenAI a provoqué dans le monde entier une prise de conscience du potentiel de l'IA générative.
Ce robot conversationnel (chatbot) permet à chacun d'accéder à un modèle à la fois :
- généraliste : il peut traiter tout type de demande, là où la plupart des modèles sont spécialisés dans une tâche précise ;
- multimodal : il peut générer différents contenus (texte, image, graphique, etc.), faire une recherche en ligne ou exécuter un programme informatique ;
- ergonomique : les échanges se font simplement (dans un chat), en langage naturel, et ne demandent aucune compétence technique particulière ;
- peu coûteux : 22 euros par mois pour le modèle le plus puissant du marché (GPT-4), gratuit pour GPT-3.5.
Quelques grands modèles de langage (LLM) concurrents de ChatGPT/GPT-44
L'ESSENTIEL
· La santé et les activités médicales, services publics essentiels qui représentent des dépenses publiques de près de 10 % du PIB en France, sont des domaines amenés à être profondément transformés par l'intelligence artificielle (IA).
· La production massive de données de santé et la complexité de leur traitement font de l'IA une aide précieuse pour la pratique médicale.
· Mais en même temps, comme à chaque saut technologique, l'apparition de risques liés aux transformations rapides pose de nombreuses questions. L'IA ouvre en particulier de nouveaux champs d'interrogations sur l'éthique, tant la perspective d'une médecine totalement mécanisée et déshumanisée paraît inacceptable.
· La technologie étant désormais disponible, il est illusoire de penser qu'on pourra échapper aux risques qu'elle comporte par des interdictions. Toute technologie performante est forcément utilisée. L'important est de créer un cadre de régulation pertinent pour l'utiliser le mieux possible. Celui-ci se met en place progressivement. L'adoption de l'AI Act à l'échelle européenne constitue à cet égard une étape importante.
· L'objet du rapport n'est pas de fournir une analyse exhaustive des technologies d'IA mises en oeuvre dans le domaine de la santé mais d'identifier les différents scénarios de déploiement de l'IA, en s'appuyant sur les utilisations déjà existantes ou celles actuellement développées par des startups en lien avec les professionnels de santé.
· Il convient d'éviter un « techno-enthousiasme » excessif, voyant dans l'IA une solution miracle et négligeant les nombreuses adaptations qui seront nécessaires, mais aussi de verser dans le « techno-pessimisme » surestimant les difficultés et les risques.
PREMIÈRE PARTIE
LES PERSPECTIVES PLEINES
DE PROMESSES DE L'IA EN SANTÉ
I. LA SANTÉ, DOMAINE PRIVILÉGIÉ DE DÉPLOIEMENT DE L'IA
A. LA SANTÉ : UN BON TERRAIN POUR L'IA
Le service public de la santé est assuré par une multitude d'acteurs qui produisent d'abondantes données médicales et administratives : médecins, hôpitaux, cliniques, laboratoires, centres radiologiques, caisses de sécurité sociale, équipes de recherche clinique...
À l'échelle de la santé individuelle, la prise en charge du patient nécessite le traitement de très nombreuses variables : outre les informations administratives et financières liées au soin, le parcours du patient se traduit par la collecte de masses de données biologiques ou physiopathologiques (rythme cardiaque, saturation du sang en oxygène), d'images (radiographies, échographies, endoscopies...), de comptes rendus d'examen clinique, de comptes rendus opératoires, de listes de médicaments délivrés, etc. Ces données doivent en outre être suivies dans le temps. La révolution de la génomique ou encore les progrès des connaissances en immunologie conduisent à brasser pour chaque patient des informations de plus en plus précises, nombreuses et complexes avant de poser un diagnostic et de mettre en place un traitement.
À l'échelle collective, l'identification des mécanismes pertinents pour traiter les différentes pathologies, les actions de santé publique destinées à améliorer l'état de santé global de la population ou à prévenir l'apparition de maladies, nécessitent aussi de brasser des quantités considérables de données et de les croiser de manière pertinente, pas seulement dans le champ du soin, mais en prenant aussi en compte des variables d'environnement : exposition aux polluants, modes de vie, comportements.
Le traitement simultané de telles masses d'informations est difficile, voire impossible pour le cerveau humain. Les professionnels de santé n'échappent pas à cette difficulté, que ce soit en recherche ou en pratique clinique. L'informatique classique a fourni une aide précieuse pour surmonter notre incapacité à traiter seuls des informations toujours plus nombreuses et variées. Des outils numériques reposant sur une IA classique, c'est-à-dire l'IA symbolique, basée sur des connaissances et appliquant des règles prédéfinies, permettent ainsi d'améliorer le travail des soignants. Cette technologie d'IA traditionnelle, connue depuis des décennies, gagne en performances avec, d'une part, l'accroissement des capacités de calcul, d'autre part, des algorithmes toujours plus perfectionnés.
Ces dernières années, les technologies d'IA connexionniste, fonctionnant par auto-apprentissage, supervisé ou non, ont permis des avancées spectaculaires en rendant possible la génération automatique de texte ou d'images par ordinateur. Dans un rapport intitulé Systèmes d'IA générative en santé : enjeux et perspectives, adopté le 5 mars 2024, l'Académie nationale de médecine estime que « leurs champs d'applications dans le domaine de la santé sont vastes et peuvent aller de l'aide à la rédaction de notes d'information à la rédaction de thèses ou de projets de programme de recherche »1(*).
Lors de son audition, la Pr Brigitte Seroussi a mis en évidence une tension entre performance et explicabilité des deux catégories d'IA : l'IA symbolique est très explicable mais a des performances limitées (elle ne produit que ce pour quoi elle a été programmée et n'invente rien) tandis que l'IA connexionniste, qui fonctionne par des rapprochements statistiques, est très performante (elle peut donner un résultat sans qu'on l'ait prévu) mais la manière de parvenir à un résultat n'est pas explicable. L'IA générative est capable de produire des contenus étonnants, d'effectuer des rapprochements auxquels on n'aurait pas forcément pensé. Elle libère donc un potentiel créatif numérique qui ouvre des champs nouveaux de réflexion.
B. LES AVANTAGES DE L'UTILISATION DE L'IA EN SANTÉ
L'IA représente un saut technologique susceptible d'améliorer le service public de la santé par une meilleure organisation des soins, faisant gagner à la fois en qualité des soins pour les patients et en temps de travail pour les professionnels. L'IA constitue ainsi un levier d'amélioration du système de santé. D'importants gains de productivité sont en particulier attendus avec le déploiement de l'IA mais le chiffrage des gains est très approximatif et la manière dont le temps gagné sera redéployé est encore très incertain.
1. Des soins de meilleure qualité
S'appuyant sur les travaux de l'OMS, qui estime que les erreurs médicales causent environ 1 décès pour 1 million d'habitants. L'Alliance européenne pour un accès à des médicaments sûrs avance une estimation pour l'Union européenne à 163 000 décès en Europe suite à une erreur médicale. La moitié des erreurs seraient liées à des médicaments2(*). Ce chiffre est fortement contesté, car il résulte d'une extrapolation à partir d'études dont certaines sont très anciennes et donnent des fourchettes très larges.
Le dernier bilan des « événements indésirables graves associés aux soins » (EIGS)3(*) publié par la Haute Autorité de santé (HAS) fait état de 2 385 EIGS en 2022, dont la moitié sont considérés comme évitables. Ces chiffres doivent être examinés avec précaution car, d'une part, tous ces événements n'ont pas causé des décès de patients (pour les incidents liés aux médicaments, le décès du patient a été constaté dans environ 30 % des cas), d'autre part, en sens inverse, les disparités régionales de déclaration suggèrent que le dispositif de signalement ne couvre pas le phénomène de manière exhaustive.
Si l'IA n'est pas une solution miracle, le déploiement d'outils l'utilisant pourrait permettre de limiter les pertes d'information, de mieux guider le déroulement d'un protocole de soins, de déclencher des alertes quand des anomalies sont repérées, et donc d'éviter les erreurs ou les mauvais choix. Lors de son audition, la société Doctolib, éditeur de logiciel d'aide à la prescription à destination des médecins, indiquait que le signalement des interactions médicamenteuses inadéquates était déjà intégré à son offre logicielle.
Par sa capacité de traitement de données nombreuses et variées, l'IA effectue des contrôles, propose des pistes diagnostiques et thérapeutiques qui enrichissent le travail médical. Le déploiement d'outils d'IA est ainsi susceptible d'harmoniser vers le haut les pratiques médicales et d'appliquer pour tous les meilleurs protocoles.
Dans une synthèse intitulée « L'IA dans le domaine de la santé, un immense potentiel, d'énormes risques », les experts de l'OCDE estiment qu'« utilisée de manière sûre et adaptée, l'IA serait en mesure d'entraîner une croissance exponentielle de la médecine fondée sur des preuves, avec à la clé de meilleurs résultats en matière de santé et des soins davantage centrés sur la personne »4(*).
L'adoption de solutions d'IA pourrait ainsi non seulement améliorer les soins, mais aussi homogénéiser les pratiques. Même s'il existe un certain tabou sur le sujet, il est évident qu'il existe des disparités de compétences entre professionnels de santé. Certains praticiens sont ainsi davantage à la pointe de leur discipline que d'autres. Il existe certes une obligation de formation continue des médecins (21 heures par an) mais sa mise en place est récente et progressive. En outre, il est évident qu'aucun praticien ne peut prétendre être omniscient. L'IA, en guidant la pratique clinique, et à condition que les logiciels d'IA soient régulièrement actualisés, constitue un instrument de standardisation des soins en s'alignant sur les meilleures pratiques.
2. Un potentiel de gain de temps pour les soignants, impossible à réellement chiffrer
Le système de santé est confronté depuis plusieurs années à un manque de temps médical et soignant, qui trouve sa traduction dans d'importants délais de rendez-vous, des fermetures de cabinets ou de services hospitaliers, et potentiellement le renoncement aux soins. Avec le vieillissement de la population et le développement inévitable de maladies chroniques, les besoins en matière de santé devraient toutefois être orientés à la hausse.
Une étude de l'OMS de 2016 estimait qu'il pourrait manquer en 2030 en Europe (UE28) 4,1 millions de travailleurs dans le secteur de la santé : 0,6 million de médecins, 2,3 millions d'infirmiers et aides-soignants et 1,3 million d'autres personnels de soins. Devant cette pénurie préoccupante de personnels qualifiés, l'enjeu de la libération du temps médical et plus largement du temps soignant est devenu majeur.
C'est là un deuxième apport de l'IA, qui pourrait intervenir pour réaliser certaines tâches chronophages et facilement automatisables. Les tâches administratives représentent une part non négligeable de l'activité des médecins et des infirmières. L'OCDE estime que 25 % du temps de travail des infirmières est consacré à saisir des données. Le temps administratif des médecins libéraux représenterait au moins 10 % de leur temps de travail5(*), certaines estimations étant encore bien plus élevées.
La priorité pourrait être donnée aux tâches pénibles et répétitives, mais pas seulement. L'IA générative est ainsi mobilisée pour automatiser la rédaction de comptes rendus médicaux ou encore pour réaliser le codage des actes (notamment le codage dans le cadre hospitalier).
Les évaluations du temps gagné sont encore assez imprécises mais ces gains de temps pourraient être très importants, tout en assurant une grande fiabilité des processus automatisés. L'OCDE, s'appuyant sur une étude de 2020, indique que « jusqu'à 36 % de l'activité des services de santé et des services sociaux pourraient être automatisés » grâce à l'IA6(*).
Un autre aspect réside dans l'accélération de la prise en charge et la réduction des délais d'attente en mettant en place des organisations plus performantes. L'installation d'un logiciel de lecture automatique des radios en cas de suspicion de fracture aux urgences du CHU de Rennes a ainsi conduit à une baisse de 30 % du délai d'attente des patients7(*).
3. Un système de santé plus efficient ?
La prise en charge de la santé représente un coût significatif dans les pays développés, en grande partie socialisé. Au sein de l'OCDE, les dépenses de santé représentaient 9,2 % du PIB en 2022, chiffre qui atteint 12,1 % en France (dont 80 % sont pris en charge par la collectivité) et 12,7 % en Allemagne8(*).
À ce coût élevé s'ajoute une certaine désorganisation de notre système de soins, dénoncée régulièrement par les professionnels, qui conduit à ne pas toujours utiliser au mieux les ressources disponibles. Gestion des effectifs, programmation des soins, enchaînement des traitements, suppression des examens redondants : l'IA est susceptible de permettre une meilleure organisation générale du processus de soins. En outre, elle peut aider à lutter contre les phénomènes de fraude (voir rapport thématique n° 1).
Rien ne dit cependant comment ces gains de temps et d'argent pourraient être utilisés : sous forme d'économies dans les dépenses de santé, sous forme d'une hausse du temps relationnel passé auprès des patients, sous forme de temps supplémentaire pour la recherche clinique, ou tout simplement pour alléger la charge de travail globale des équipes soignantes.
II. UNE UTILISATION QUI RESTE ENCORE PRINCIPALEMENT EXPÉRIMENTALE
A. DE NOMBREUX DOMAINES D'APPLICATION POSSIBLES
1. L'intelligence artificielle, accélérateur de la recherche médicale
La pandémie de covid-19 a montré l'intérêt d'une mobilisation de toutes les technologies disponibles pour faire face à un besoin de recherches très rapides. Dans ce contexte, l'IA peut se révéler très précieuse. Ainsi, l'identification de la structure en trois dimensions de protéines extrêmement complexes9(*) ouvre la voie à l'élaboration accélérée de vaccins efficaces. L'IA peut également aider à prédire l'évolution de la pandémie et appuyer les équipes soignantes dans l'identification du virus chez les patients10(*).
Comme l'indique le rapport de l'Académie nationale de médecine sur les systèmes d'IA générative, « la recherche se heurte aujourd'hui aux limites de nos capacités intellectuelles à colliger, organiser et donner du sens à des données massives et hétérogènes d'origines variées ». L'IA générative vient donc à point pour permettre « une augmentation de l'efficacité, de la précision et de la vitesse à laquelle les données peuvent être générées, analysées et partagées ».
L'IA ouvre de nouvelles perspectives à l'industrie pharmaceutique à travers plusieurs leviers11(*) :
- elle permet d'accélérer l'identification des molécules candidates : le criblage des molécules cibles se fait par voie computationnelle de manière rapide, parfois en quelques heures. L'IA aide ainsi à prédire l'activité médicamenteuse d'une molécule, par exemple à travers la modélisation de sa capacité à reconnaître une cible (protéine, ARN) et à s'y insérer12(*) ;
- elle simplifie la gestion des essais cliniques : l'analyse des dossiers médicaux peut être largement automatisée, la sélection des groupes de patients pertinents pour la recherche peut s'effectuer sur une base plus large, les groupes de contrôle peuvent être réduits, voire remplacés par des groupes contrôles synthétiques. Le recours aux jumeaux numériques constitue notamment une piste féconde pour limiter le nombre de patients à inclure dans une recherche clinique ;
- elle permet aussi de mettre en relation davantage d'informations, et selon les termes du rapport de l'Académie de médecine précité « ouvre la voie aux études systémiques nécessaires à notre compréhension des maladies multigéniques et multifactorielles qui sont la conséquence d'interactions entre génotype, phénotype et environnement » ;
- elle renforce la pharmacovigilance, en permettant une analyse plus fine et plus rapide de données en vie réelle.
Pour la recherche médicale, la mobilisation de l'IA présente un double intérêt :
- elle réduit les coûts des recherches, alors que ceux-ci ont explosé depuis une vingtaine d'années ;
- elle diversifie les possibilités de recherche, en permettant de s'intéresser davantage aux maladies rares.
À rebours de la tendance à la concentration de la recherche médicale autour de quelques grands groupes, ciblant essentiellement des pathologies chroniques qui touchent un très grand nombre de malades dans le monde, afin de pouvoir amortir des coûts de recherche très importants, l'IA pourrait favoriser un foisonnement de la recherche médicale par la multiplication de ses acteurs et la diversification de ses domaines.
Des précautions importantes sont cependant nécessaires pour faire face aux inconvénients de l'IA dans la recherche en biologie et santé. La production automatique de résultats est ainsi dépendante des données disponibles. Des données falsifiées peuvent conduire à la production de résultats erronés, dont le système d'IA peut ne pas se rendre compte, faute de capacité d'analyse. Par ailleurs, la recherche scientifique passe par la revue par les pairs et la reproduction d'expériences pour valider les résultats obtenus. Or, l'IA générative ne permet pas d'expliquer les résultats, ou de produire une bibliographie.
2. L'imagerie médicale en pleine révolution
L'imagerie médicale fournit aux médecins une visualisation de parties internes du corps humain dont l'interprétation est décisive pour fournir un diagnostic et proposer des traitements aux patients. La lecture des clichés est un exercice ardu pour les radiologues, qui dépendent pour leur travail de la qualité des images fournies et doivent aussi porter leur attention sur des petits détails pas toujours faciles à identifier.
L'imagerie médicale constitue un domaine où la dimension technique est présente depuis de nombreuses années, avec des appareils qui n'ont cessé de se perfectionner. La numérisation des clichés radiologiques pris par les appareils de radiologie médicale, scanners, IRM, a ouvert la voie au traitement automatique des images par des algorithmes de plus en plus performants.
L'IA permet en effet d'améliorer la qualité des images fournies par les appareils mais aussi de les interpréter de manière automatique, ou du moins de signaler des anomalies devant faire l'objet d'une analyse approfondie.
La preuve de la performance des systèmes à base de réseaux de neurones convolutifs profonds dans la reconnaissance d'images, apportée par des chercheurs américains en 201213(*), a donné un coup d'accélérateur aux applications de technologies d'IA en imagerie médicale14(*). Désormais, de nombreuses solutions à base d'IA sont proposées aux médecins et professionnels de santé, avec comme objectifs à la fois de faire gagner du temps dans la réalisation des examens et la lecture des clichés mais aussi de mieux détecter les zones d'intérêt. Gagner en rapidité et en efficacité faisait dire en 2016 à Geoffrey Hinton, lauréat du prix Turing 2018 qu'on devrait arrêter de former des radiologues puisque le deep learning allait faire mieux qu'eux à brève échéance.
En réalité, ce remplacement des radiologues par les machines ne s'est pas produit. Certes, les logiciels d'interprétation d'images automatisée se sont multipliés : mi-2022, plus de 200 logiciels avaient été validés par la FDA aux États-Unis ou bénéficié d'un marquage CE dans l'Union européenne15(*) (au total environ 700 dispositifs médicaux intégrant l'IA ont été validés par la FDA). Mais leurs apports sont fortement questionnés. De nombreuses voix s'élèvent pour appeler à ne pas surestimer leur rôle. Les promesses sur le papier ne sont d'ailleurs suivies que d'une application clinique limitée16(*). Par ailleurs, même dans des domaines où l'IA se révèle performante, elle n'est pas forcément plus performante qu'un radiologue expérimenté.
Selon une étude britannique publiée en septembre 2023, pour des mammographies de dépistage du cancer du sein, les résultats obtenus par un oeil humain et par un algorithme sont similaires17(*).
L'IA peut donc être utilisée dans ce cadre non comme un substitut, mais comme une aide pour le praticien, capable de lui fournir un premier tri dans la masse des éléments à analyser sur un cliché. En réalité, c'est la combinaison d'un examen classique et de l'utilisation d'IA qui pourrait apporter des gains de temps et de performance significatifs.
L'usage de l'intelligence artificielle dans le dépistage organisé du cancer du sein
Depuis 2004, la France s'est dotée d'un dispositif de dépistage organisé (DO) du cancer du sein. Avec plus de 60 000 cas par an et un peu plus de 12 000 décès par an, le cancer du sein est à la fois le plus fréquent et le plus meurtrier pour les femmes. Un dépistage précoce améliore considérablement le taux de survie à 5 ans, qui s'établit désormais à 87 %.
Le DO consiste à inviter toutes les femmes de 50 à 74 ans à passer un examen de dépistage tous les deux ans, pris en charge à 100 % par l'assurance maladie. L'examen comprend une mammographie et un examen clinique. Un peu moins de 50 % des femmes concernées utilisent ce dispositif, s'ajoutant aux 11 % de femmes procédant à un dépistage dans une démarche individuelle.
Lorsqu'aucune anomalie n'est décelée, un second examen est réalisé par un radiologue expert (double lecture). Depuis 2019, les mammographies sont exclusivement numériques. Les clichés sont pris en 2 dimensions, mais devant les performances de la tomosynthèse18(*), la Haute Autorité de santé (HAS) a recommandé en 2023 l'intégration de cette nouvelle technique qui permet d'obtenir une image reconstituée en 3 dimensions grâce à des algorithmes mathématiques19(*).
Le déploiement d'outils d'IA pourrait augmenter l'efficacité globale du DO du cancer du sein et conduire à le réorganiser, mais la bonne manière d'utiliser ces nouvelles possibilités est discutée par la communauté scientifique.
Début 2024, la Société d'imagerie de la femme (SIFEM)20(*) a mis en avant 3 études prospectives :
- une étude suédoise (MASAI) montrait que l'utilisation de l'IA pour une première lecture augmentait le taux de détection des cancers (sans augmentation des faux positifs) et diminuait fortement la charge de travail des radiologues ;
- une autre étude suédoise (ScreenTrustCAD) montrait qu'utilisée en deuxième voire troisième lecture, l'IA augmente le nombre de cancers détectés et diminue le nombre de mammographies nécessitant un bilan complémentaire (échographie, biopsie, chirurgie) ;
- une étude hongroise, enfin, mettait en évidence une amélioration du taux de détection des cancers grâce à l'utilisation d'une IA en troisième lecture.
Si l'utilisation de l'IA en remplacement des radiologues n'est pas envisageable pour des raisons éthiques et parce que la performance des radiologues experts paraît encore supérieure à la machine aujourd'hui, la combinaison d'une lecture humaine et d'une lecture par IA des mammographies permettrait vraisemblablement de gagner en temps et en efficacité.
Dans une tribune publiée par Le Monde le 4 avril 2024, un collectif de radiologues insistait sur la nécessité de s'organiser pour pouvoir accueillir ces nouveaux instruments, dans un cadre technique et organisationnel maîtrisé21(*).
3. Vers un déploiement de l'IA « tous azimuts »
Au-delà de l'imagerie, domaine pionnier du déploiement de l'IA en santé, le potentiel de l'IA s'applique à la totalité des champs de l'activité clinique.
L'IA peut ainsi être utilisée tant dans la phase de dépistage ou de détection (diagnostic) que dans la phase de mise en oeuvre de solutions thérapeutiques.
En ophtalmologie, l'IA crée la possibilité de détection précoce de certaines pathologies, comme la rétinose diabétique, l'oedème maculaire diabétique, la dégénérescence maculaire ou encore le glaucome.
En cancérologie, l'IA peut être sollicitée dans le dépistage et la détection précoce, permettant de mettre en évidence des anomalies plus rapidement et donc d'améliorer la prise en charge ultérieure des patients. Lors de son audition, l'Institut national du cancer (INCa) a indiqué que l'IA était utilisée par exemple pour détecter des polypes ou adénomes par coloscopie, ou pour mieux détecter par scanner les cancers du poumon. On manque toutefois de certitudes sur la plus-value apportée par ces outils. L'INCa estime qu'il existe un énorme potentiel de l'IA en diagnostic de jeux de données sur les tumeurs, notamment en matière de radiomique et en génomique, dans la définition de scores en vue d'une personnalisation des approches, ou encore pour le criblage d'anomalies moléculaires.
Le large champ d'application de l'IA en cancérologie
Les domaines d'intervention de l'IA en cancérologie sont multiples et variés. Lors de son audition, l'Institut national du cancer (INCa) en a donné de nombreux exemples.
1 - Interventions de l'IA lors du diagnostic et de la détermination du stade du cancer
· Recours à l'IA pour la lecture d'images :
- diagnostic du cancer primitif : radiologie (sein, poumon, thyroïde, prostate), photos (mélanomes), lames d'anatomopathologie numérisées ;
- recherche de métastases ;
- recherche de mutations ou expression de marqueurs histologiques : attribuer les mutations à partir d'images (histologie ou imagerie), plus spécialement pour les mutations qui conditionnent le choix d'un traitement, pourrait s'avérer plus rapide et moins coûteux que le séquençage ;
- attribution de scores, par exemple attribution du score de Gleason à partir de l'IRM pour le cancer de la prostate ;
· Assistance à la détection de polypes/cancers en coloscopie ;
· Identification du cancer primitif pour des métastases de cancer primitif inconnu grâce au profil génétique des cellules métastatiques ;
· Analyse de données massives permettant l'identification de sous-groupes homogènes (clustering), par exemple pour réaliser l'intégration de données génomiques dans la stratification des cancers.
2 - Interventions de l'IA lors du choix du traitement
· Réalisation de modèles prédictifs pour évaluer ex ante l'efficacité de diverses options thérapeutiques permettant de guider le choix du traitement. À partir des images de tomodensitométrie, on peut ainsi identifier parmi les personnes ayant des métastases hépatiques d'un cancer colorectal, celles qui sont susceptibles de répondre au traitement médicamenteux systémique. On peut aussi prédire la réponse thérapeutique à la combinaison atezolizumab/bevacizumab dans le carcinome hépatocellulaire à partir de l'analyse des lames histologiques digitales ;
· Prédiction de la survenue de complications après traitement (radiothérapie, immunothérapie) permettant d'adapter la surveillance.
· Les outils d'aide à la décision thérapeutique résultant de la mise en oeuvre des modèles prédictifs constituent un pas de plus vers une médecine personnalisée.
3 - Interventions de l'IA dans le traitement lui-même
· En radiothérapie : pour affiner le ciblage de la zone à irradier en assistant le détourage, pour anticiper le mouvement des organes durant la respiration et compenser ces mouvements pendant le traitement, permettant d'améliorer le ciblage vers la tumeur, pour adapter le traitement au fil des semaines en fonction des modifications subies par le corps en raison, par exemple, d'un amaigrissement ;
· En chirurgie : recours à la chirurgie assistée par ordinateur ;
· Dans le suivi du patient : détection de signaux par la pharmacovigilance, identification des seconds cancers, complications, séquelles à moyen ou long terme. Il existe désormais des applications numériques pour le suivi des patients ou la surveillance à domicile en cours de traitement, y compris pour des personnes incluses dans des essais thérapeutiques.
4 - Interventions de l'IA dans la recherche
· Appui à la recherche de nouvelles molécules ;
· Constitution de bras de contrôle synthétiques en recherche clinique ;
· Réalisation d'essais in silico c'est-à-dire création de patients virtuels et simulation d'essais cliniques sur ces cohortes virtuelles.
5 - Interventions de l'IA pour l'analyse de données en vie réelle
· Analyse de trajectoires de soins, du pré-diagnostic jusqu'à la fin de vie ;
· Vérification de l'application des recommandations de soins ;
· Possibilité de mener des études sur une population non sélectionnée (contrairement à celle des essais cliniques) pour documenter l'utilisation des médicaments en vie réelle, vérifier l'efficacité en condition réelle sur des critères mesurables par ce type de données, en tenant compte de l'absence de randomisation et apprécier la tolérance sur des populations quasi exhaustives.
En anatomopathologie, l'IA est sollicitée pour l'interprétation histologique (examen de la structure des coupes de pièces anatomiques), la prédiction d'anomalies moléculaires à partir des caractéristiques morphologiques constatées sur les lames numérisées ou encore la prédiction des réponses aux traitements.
En neurologie, l'IA peut être utilisée dans la phase diagnostique, mais intéresse aussi la phase thérapeutique. La rééducation des fonctions neuronales après un accident vasculaire cérébral (AVC) peut ainsi être aidée par des machines s'adaptant aux progrès du patient. Par ailleurs, les implants neuronaux destinés à compenser des fonctions déficientes ou à augmenter les capacités humaines sont aujourd'hui en développement.
En cardiologie, l'IA peut aussi apporter beaucoup, d'autant plus qu'il faut souvent diagnostiquer et traiter rapidement les douleurs thoraciques ou les arythmies cardiaques, dès leur apparition. L'insuffisance cardiaque connaît un taux important d'erreurs - une étude britannique publiée en 2016 estimait qu'une crise cardiaque sur trois était mal diagnostiquée22(*).
En outre, certaines défaillances cardiaques sont difficilement repérables. L'IA peut aider à identifier une dysfonction ventriculaire gauche asymptomatique ou encore une fibrillation auriculaire silencieuse à partir d'un simple électrocardiogramme. Le traitement des données des pacemakers connectés offre aussi un instrument supplémentaire de surveillance en temps réel des patients atteints de pathologie cardiaque.
En néphrologie, l'IA a également permis de réels progrès. Lauréat du prix Innovation 2023 de l'Inserm, le professeur Alexandre Loupy, responsable de l'Institut de transplantation de Paris23(*) a développé un algorithme capable d'analyser de très nombreuses données (génétiques, anticorps, biomarqueurs) permettant de prédire les risques de rejets des greffons et ainsi d'améliorer leur appariement avec les greffés. Il en résulte un moindre gâchis des greffons, ceux-ci étant structurellement en pénurie, mais aussi une réduction des traitements immunosuppresseurs, pour le plus grand bénéfice à long terme des patients.
Neurotechnologies et IA : vers un homme augmenté ?
Les neurotechnologies (NT) étudient le cerveau et développent des technologies pour interagir avec lui, visant à améliorer son fonctionnement. Selon le Comité international de bioéthique de l'Unesco (CIB), elles englobent tous les dispositifs et procédures pour visualiser, surveiller, étudier, manipuler et reproduire la structure et le fonctionnement des systèmes neuronaux humains24(*).
Les NT se sont avérées très prometteuses dans la réparation de certains handicaps, en particulier ceux d'ordre sensoriel. Par exemple, l'utilisation de neuroprothèses, constituées de capteurs d'informations et d'un processeur les convertissant en stimuli électriques, permet de transmettre des informations sensorielles au cerveau via des électrodes lorsque l'organe normal est défaillant.
De même, l'exemple de la stimulation cérébrale profonde (Deep Brain Stimulation - DBS) illustre parfaitement comment les neurotechnologies peuvent être bénéfiques pour la médecine. Cette technique, consistant à implanter des électrodes de stimulation dans des noyaux profonds du cerveau et à les relier à deux piles électriques implantées au niveau sous-claviculaire pour délivrer un courant continu de faible intensité, est utilisée avec succès dans le traitement de la maladie de Parkinson. Elle permet de mimer des microlésions dans des structures cérébrales choisies et ainsi de réduire les tremblements de 80 %, et pourrait également être appliquée à d'autres maladies telles que la maladie d'Alzheimer, ainsi qu'à des troubles psychiques25(*).
Récemment, les chercheurs ont tenté d'associer les NT et l'IA, offrant des perspectives diverses. D'une part, les NT couplées à l'IA peuvent améliorer leur efficacité. C'est le cas par exemple de la création d'un exosquelette, ayant pour objectif de compenser une fonction absente ou défaillante chez un patient. En 2019, dans le cadre du projet Brain Computer Interface, Clinatec a développé une neuroprothèse capable de contrôler un exosquelette par la pensée. Cette neuroprothèse, testée sur un homme tétraplégique souffrant d'une lésion de la moelle épinière, capte les signaux électriques émis par le cerveau lors d'une intention de mouvement. Ces signaux sont ensuite interprétés par un ordinateur grâce à l'IA, utilisant la technique du neurofeedback, puis renvoyés à l'exosquelette pour effectuer le mouvement « pensé »26(*).
D'autre part, l'IA et les NT ouvrent de nouveaux horizons, notamment celui de l'homme augmenté. Les investissements dans le domaine des NT ont augmenté de 700 % entre 2014 et 202127(*), car l'hybridation du cerveau avec l'IA semble de plus en plus réalisable. Elon Musk, pionnier dans ce domaine, a fondé Neuralink en 2017, avec pour objectif principal d'améliorer les capacités cognitives de l'homme grâce à des implants et à l'IA, et ainsi créer un véritable homme augmenté.
Le concept d'homme augmenté présente des limites et soulève des défis éthiques majeurs. L'utilisation de l'IA dans les NT peut entraîner des risques d'efficacité inégale, de complications liées à l'implantation des électrodes (telles que des hémorragies, des dysfonctionnements ou des crises d'épilepsie), voire altérer la personnalité du patient et accentuer les inégalités sociales, puisque l'accès aux NT est souvent réservé aux plus fortunés. L'ensemble de ces risques s'accompagne de préoccupations éthiques, comme la protection des données personnelles, la sauvegarde de l'intégrité de la personne et le respect du libre arbitre.
Face à ces enjeux, l'évolution des « neurodroits » est essentielle. Le groupe d'experts ad hoc de l'Unesco recommande notamment la création d'un concept d'intimité mentale. En France, le cadre juridique reste encore peu développé : il interdit simplement la modification de l'activité cérébrale si cela présente un danger, et limite l'utilisation de l'imagerie cérébrale à des fins médicales ou de recherche.
L'évolution rapide des NT et de l'IA soulève une question fondamentale : devons-nous les utiliser uniquement dans un cadre médical strict, ou devrions-nous explorer les frontières de l'humain et tenter de créer un être augmenté ?
Auditionné par la délégation à la prospective, le Pr Raphaël Gaillard, chef du pôle hospitalo-universitaire de psychiatrie de l'hôpital Sainte-Anne, indique ne pas croire à la possibilité d'augmenter l'ensemble des fonctions de l'homme de manière homogène, tant les zones du cerveau sont nombreuses et variées et les implants neuronaux spécialisés dans leurs fonctions et localisation. Il plaide en faveur de la première option et met en garde contre les dangers d'une utilisation excessive des NT : « Au-delà de la question de la réparation, l'augmentation de l'homme ne peut se faire que de façon non harmonieuse, je dirais même, c'est un terme de psychiatrie, dysharmonique, c'est-à-dire ne respectant pas l'harmonie initiale que nous confère la biologie de notre cerveau. En augmentant l'homme suivant ce Silicon syndrome, nous renonçons à l'harmonie de l'homme, et ce n'est pas rien comme changement anthropologique »28(*).
B. UNE UTILISATION EN ROUTINE POUR LE SOIN ENCORE LIMITÉE
Il existe donc un grand nombre de domaines d'application de l'IA en santé. Pour autant, hors imagerie, l'IA n'est pas encore utilisée en routine. La pratique clinique n'a pas encore totalement intégré ce progrès technique récent. Nous connaissons donc un foisonnement d'expérimentations, mais pas encore une banalisation des nouveaux outils.
Plusieurs obstacles retardent en effet le déploiement de l'IA en santé : l'un d'entre eux est le manque de recul et la méfiance que l'IA peut susciter à la fois chez les professionnels de santé et chez les patients. Certes, selon une étude publiée début 202429(*), 58,7 % d'entre eux affirment avoir confiance en l'IA pour l'aide au diagnostic et à la prise en charge et 66,6 % estiment qu'elle ne constitue pas une menace pour leur profession ou leurs compétences. Si 53 % des professionnels interrogés affirment utiliser l'IA dans leur pratique quotidienne, il s'agit surtout d'aller chercher de l'information médicale ou de se former. Nous sommes donc encore loin d'une délégation quasi complète de certaines tâches à l'IA.
Du côté des patients, seulement 44 % d'entre eux estiment possible de se faire soigner par leur médecin à l'aide d'une IA, selon un sondage Opinionway réalisé en 2023 pour le Healthcare Data Institute30(*). Il reste donc du chemin pour faire entrer le recours à l'IA dans les pratiques habituelles de soin.
Un autre obstacle réside dans les incertitudes réglementaires et l'absence de modèle économique pour nombre de dispositifs médicaux numériques (DMN). Les dispositifs individuels peuvent bénéficier d'un remboursement et, de fait, des mécanismes d'accès rapide au remboursement ont été mis en place à titre expérimental. Pour les logiciels et équipements intégrant des solutions d'IA et utilisés en cabinet médical ou en établissement de santé, ils doivent trouver d'autres sources de financement : soit sur fonds propres soit en mobilisant des outils d'aide à l'innovation, tel le fonds pour l'innovation du système de santé (Fiss) créé par la LFSS de 2018.
Lorsque les gains de productivité apportés par la solution à base d'IA sont évidents, l'investissement peut s'autofinancer, mais lorsque les gains sont incertains, il faut financer les nouveaux outils sur ressources propres. Les appels à projets permettent un amorçage, mais n'apportent pas des ressources pérennes de fonctionnement. Les coûts du déploiement de l'IA peuvent ainsi constituer un frein à une utilisation en routine sans gain de productivité apparent net. La Fédération hospitalière de France (FHF) ajoute que « beaucoup de services IA sont basés sur un modèle de financement à l'usage, ce qui pèse sur le budget d'exploitation et ce qui est très difficile à maîtriser sur le plan budgétaire ».
Le cadre juridique et tarifaire des dispositifs médicaux numériques (DMN)
La mise sur le marché des dispositifs médicaux numériques (DMN) comme par exemple des logiciels d'aide au diagnostic ou de surveillance, est soumise à une procédure de marquage CE obtenu suite à une certification délivrée par un organisme indépendant appelé « organisme notifié ». Les conditions du marquage varient selon la classe de risque du dispositif. C'est l'Agence nationale de sécurité du médicament (ANSM) qui est chargée de la surveillance de l'ensemble des dispositifs médicaux.
Après l'étape du marquage CE, les DMN sont soumis à la Commission nationale d'évaluation des dispositifs médicaux et des technologies de santé (CNEDiMTS), dépendant de la Haute Autorité de santé (HAS), qui formule un avis avant inscription du dispositif sur la liste des produits et prestations remboursables (LPPR) ou sur la liste des activités de télésurveillance médicale (LATM), au vu notamment de l'amélioration du service attendu.
Le processus d'inscription pérenne sur la LPPR ou la LATM étant long, il existe une procédure de prise en charge anticipée des DMN innovants et une procédure de prise en charge transitoire pour des produits de santé présumés innovants.
Pour les dispositifs médicaux à usage individuel, l'admission au remboursement est suivie de la fixation d'un tarif de remboursement par le Comité économique des produits de santé (CEPS).
Afin de garantir que les DMN effectuant un traitement de données à caractère personnel au sens du règlement général sur la protection des données (RGPD) assurent un degré suffisant de protection des données personnelles, ils doivent par ailleurs obtenir un certificat de conformité au référentiel d'interopérabilité et de sécurité des dispositifs médicaux numériques délivré par l'Agence du numérique en santé (ANS).
Au final, l'IA est en train de s'installer comme une réalité nouvelle dans le domaine de la santé, mais sans généralisation ni banalisation complète. Le degré de maturité des cas d'usage de l'IA en santé est en outre disparate selon les domaines, comme le montre la dernière analyse du Healthcare Data Institute :
C. UN POTENTIEL DE TRANSFORMATION PROFONDE DU SERVICE PUBLIC DE LA SANTÉ
1. La possibilité de bouleversements organisationnels
Au-delà de l'acte de soin, l'irruption de l'IA dans le champ de la santé ouvre la voie à des transformations importantes du système de santé lui-même et de son organisation.
Plusieurs exemples montrent que l'IA peut aider à mieux organiser la chaîne de soins, en automatisant certaines tâches fastidieuses et parfois mal exécutées. L'IA aide ainsi à la gestion des plateaux d'imagerie (solution Intuitus) dans quatre établissements de santé du pôle d'imagerie médicale mutualisé basco-landais (PIMM), à la réalisation de plannings médicaux et paramédicaux par les cadres de santé (solution Hopia), prédit le volume d'activité des urgences à J-5 au centre hospitalier de Valenciennes (solution Sania), prédit la disponibilité des lits dans les services. Pour les activités de consultation médicale, l'IA est déjà capable d'assurer le traitement des prises de rendez-vous ou encore de gérer la facturation.
Dans le domaine documentaire, l'IA peut également être très utile. Des solutions existent ainsi pour retranscrire les échanges entre patient et médecin à partir d'une reconnaissance vocale, ou encore pour mettre en forme des données collectées de manière non structurée, ou pour produire de manière semi-automatique des comptes rendus médicaux. L'activité de secrétariat médical, déjà fortement transformée depuis quelques années, pourrait de nouveau être bouleversée.
L'IA offre aussi l'opportunité de mieux traiter les flux de patients, en faisant davantage le tri entre les entrées urgentes et celles qui le sont moins. Cette fonction, essentielle aux services d'urgence, est déjà déployée dans certains établissements de santé.
L'IA peut aussi être sollicitée pour guider les professionnels dans les démarches administratives et le suivi des patients. Ainsi, au sein de l'AP-HP, le logiciel Watson sert à guider les utilisateurs du dossier médical informatisé : il repère les erreurs de saisie, émet des alertes, et sa fonction chatbot permet de répondre aux interrogations des professionnels. L'IA facilite l'appropriation des procédures complexes en milieu hospitalier.
La numérisation de la santé ouvre enfin la voie à la possibilité de faire de la médecine à distance : derrière la téléchirurgie qui permet de réaliser des opérations à distance, mais qui reste exceptionnelle, existe une large palette de solutions de télémédecine. Avec ou sans IA, la télémédecine affranchit de la contrainte physique d'une présence des patients et des soignants au même endroit. Elle constitue une réponse possible au problème des déserts médicaux.
L'IA, opportunité pour lutter contre les déserts médicaux ?
Les inégalités territoriales d'accès aux soins constituent une préoccupation croissante dans un contexte de pénurie de personnels médicaux. Un rapport d'information sénatorial d'avril 202231(*) signalait que désormais 30,2 % de la population vivait dans une zone d'intervention prioritaire (ZIP), c'est-à-dire dans un « désert médical ». Le phénomène s'aggrave (la proportion était de 18 % il y a une décennie) et touche à la fois des territoires ruraux et des territoires périurbains (en Île-de-France, 62,4 % de la population francilienne est concernée par une offre de soins insuffisante ou des difficultés dans l'accès aux soins).
Des solutions numériques peuvent apporter une réponse partielle à cette problématique et des cabines de télémédecine ont fait leur apparition depuis quelques années. On en compterait aujourd'hui environ 5 000, majoritairement situées au sein des officines de pharmacie. Les téléconsultations représentent désormais 4 % de l'ensemble des consultations en médecine de ville.
Si la téléconsultation permet d'avoir accès à un médecin à distance, sans avoir besoin de se déplacer jusqu'à un cabinet éloigné du domicile, elle ne règle cependant pas la question de la pénurie de temps médical. En outre, elle ne permet pas d'effectuer les mêmes examens cliniques (auscultation) que lors d'un rendez-vous classique.
Pour réduire la fracture dans l'accès aux soins, encore faut-il aussi réduire la fracture numérique : la télémédecine suppose l'achèvement d'une couverture numérique de bonne qualité de l'ensemble du territoire.
L'IA peut être intégrée aux solutions de télémédecine pour en améliorer les performances, en interprétant en direct des données captées dans les cabines de télémédecine ou en guidant l'entretien avec le patient. Cette aide n'est pas forcément très différente de celle fournie par les mêmes solutions d'IA déployées au sein d'un cabinet médical. Elle peut cependant être encore plus utile en télémédecine, en réduisant les inconvénients de cette pratique par une meilleure prise en compte des données médicales collectées, en encore en accélérant les temps d'examen clinique, ce qui, au final, fait gagner du temps médical.
L'IA constitue donc potentiellement un outil de meilleure organisation du processus de soins et de réduction des inégalités territoriales de santé, mais ne règle pas à elle seule la question des déserts médicaux. La nécessité d'un échange direct entre le patient et le médecin impose un maillage territorial plus équilibré de l'implantation des cabinets médicaux.
2. Vers une médecine prédictive et personnalisée
L'IA offre une capacité pour mieux anticiper les évolutions des maladies, à l'échelle individuelle des patients comme à celle des populations, mais aussi pour prévenir leur apparition, notamment par des dépistages, au service d'une amélioration de la santé publique. On pourrait ainsi passer d'une médecine principalement curative à une médecine préventive, grâce à des outils de médecine prédictive et de plus en plus personnalisée. La combinaison des progrès de la génomique et du traitement de données massives permet d'affiner l'analyse de la situation sanitaire actuelle et future de chaque individu.
Dans un rapport récent32(*), le Healthcare Data Institute souligne que la prévention et la détection des cancers sont les premiers cas d'usage préventifs de l'IA. De nouveaux algorithmes intègrent des sources de données multiples - imagerie satellite, recherches sur Internet, données des objets connectés - pour affiner les prédictions. Le rapport note que « cette capacité de prévention est permise car l'IA apporte la “couche d'adaptation” à l'accès aux modèles prédictifs ».
Mais l'apport de l'IA ne se limiterait pas à la prédiction de l'apparition de maladies. L'IA pourrait aussi prédire la réponse aux traitements et offrir de nouvelles possibilités de personnalisation des traitements.
Le revers de la médaille du développement de la médecine prédictive pourrait consister en une inflation diagnostique ou un surdiagnostic. Le surdiagnostic désigne le diagnostic d'un problème qui, s'il n'avait pas été trouvé, n'aurait pas causé de symptômes ni de décès. Autrement dit, c'est la détection d'un problème sans qu'il y ait de bienfaits possibles à tirer du traitement précoce de la personne concernée33(*). Il conduit à une surconsommation médicale et à une potentielle dégradation de l'état de santé des personnes surdiagnostiquées, celles-ci étant exposées aux effets secondaires de traitements peu utiles ou à un stress lié à leur connaissance de leur exposition à une maladie future.
Une autre transformation à anticiper est celle de la relation entre patient et médecin. D'ores et déjà, des plateformes d'information médicale, comme la plus connue Doctissimo, apportent une information médicale générale autrefois inaccessible aux non-médecins. D'autant mieux renseignés qu'ils sont directement concernés par la pathologie ou celle de leurs proches, les patients ne sont plus des ignorants soumis à la toute-puissance médicale, mais des partenaires dans le choix des traitements et du parcours de soin. Avec une IA accessible directement par les patients, ces derniers pourront être amenés à analyser eux-mêmes leur situation et à débattre avec les médecins des meilleures solutions thérapeutiques à mettre en oeuvre.
La technologie est d'ailleurs mise à contribution pour un suivi « passif » du patient : l'application de télésurveillance Oncolaxy, utilisée par l'Institut Gustave Roussy, s'appuie sur les symptômes signalés par le patient pour détecter automatiquement des rechutes ou des complications liées aux traitements suivis. Des ajustements de traitement plus rapides sont ainsi possibles.
3. Vers une remise en cause du modèle d'assurance sociale classique ?
L'assurance maladie fonctionne selon le principe de la mutualisation des risques entre assurés sociaux. L'irruption de l'IA la confronte à des défis nouveaux. Un premier défi est celui de la tarification des actes : sera-t-il acceptable de payer le même montant pour un acte réalisé par une machine et pour un acte médical réalisé par un professionnel ?
Cette question peut néanmoins trouver une solution car la prise de décision ne peut éthiquement être laissée à la machine. L'enjeu sera celui du bon niveau de tarification et de la redistribution des effets du progrès technique à travers des baisses de tarifs.
Un autre enjeu bien plus fondamental réside dans le déchirement du « voile d'ignorance » des risques individuels derrière lequel nous sommes encore cachés aujourd'hui. L'IA facilitant la quantification de nombreux aspects de la vie des individus et permettant de croiser de très nombreuses données, la gestion des risques change de paradigme. On passe d'une évaluation du risque par grand agrégat sociodémographique dans les modèles actuariels utilisés notamment par les assurances complémentaires, à une évaluation du risque plus fine, possible à l'échelle des individus, en observant bien plus attentivement ses antécédents ou encore son comportement.
Comme le note le rapport Enjeux de l'intelligence artificielle en santé de la Chaire Santé de SciencesPo, publié en 2023, « l'individualisation potentielle de l'offre assurantielle permise par l'IA mène à une responsabilisation grandissante des assurés, avec l'application possible de pénalités et l'individualisation de la tarification des primes d'assurance. Cette approche cherche donc à cerner le prix exact du risque, ce qui renverse les théories classiques sur l'assurabilité du risque et de sa mutualisation. Dans la continuité de cette logique, les assureurs pourraient ne plus être circonscrits au remboursement de la médecine curative mais devenir acteurs de la santé de leurs assurés, des financeurs de médecine préventive pour faire diminuer les risques et in fine réaliser des économies. »
DEUXIÈME PARTIE
EFFICACITÉ ET
ÉTHIQUE,
LES DEUX PILIERS DE L'ACCEPTABILITÉ
DE L'IA EN
SANTÉ
I. LA NÉCESSITÉ DE DISPOSER DE DONNÉES NOMBREUSES ET FIABLES
Le traitement des patients, de la compréhension des mécanismes biologiques propres à chaque pathologie jusqu'au choix des stratégies thérapeutiques et au suivi de leurs résultats, produit une quantité considérable de données de santé extrêmement variées, médicales et administratives.
À l'inverse de l'IA classique, symbolique, qui applique des algorithmes prédéfinis, l'IA générative a besoin d'immenses quantités de données pour apporter ses propres réponses, non prévues à l'avance. L'abondance des données de santé peut naturellement en faire un domaine privilégié du déploiement de solutions à base d'IA générative.
Encore faut-il que l'utilisation des données de santé soit possible et que celles-ci soient non seulement nombreuses, mais aussi de suffisamment bonne qualité.
A. L'ENJEU DE L'ACCÈS AUX DONNÉES SECONDAIRES DE SANTÉ
En matière d'accès aux données médicales, l'enjeu est de pouvoir utiliser les données secondaires de santé. Le rapport Marchand-Arvier publié en décembre 202334(*) distingue l'utilisation primaire des données de santé, qui renvoie à la collecte de données à l'occasion de la prise en charge des patients, tandis que l'usage secondaire désigne l'utilisation de ces données pour d'autres finalités comme la recherche et l'innovation, le pilotage ou encore l'amélioration de la qualité des soins.
La France dispose de nombreuses données primaires de santé regroupées au sein du système national des données de santé (SNDS), comprenant notamment la base de données des différents régimes d'assurance maladie (SNIIRAM), établie à partir des feuilles de soins, comprenant des données médico-administratives (mais pas de données cliniques), la base des hôpitaux (PMSI) ou encore la base des causes de décès de l'Inserm (CépiDC). Mais certaines données de santé ne figurent pas dans le SNDS : elles sont dans des entrepôts de données de santé (EDS) des établissements, dans les bases des cohortes constituées pour des recherches ou encore dans divers registres.
L'utilisation des données secondaires de santé est indispensable au développement de solutions à base d'IA. Or, comme l'indique le rapport Marchand-Arvier, elle se heurte à plusieurs freins.
· Premier frein pour les acteurs économiques comme pour les chercheurs : l'éparpillement des bases de données, leur contenu hétérogène et leur documentation insuffisante. Il n'existe pas de cartographie transverse et à jour des bases de données de santé utilisables, susceptible de renvoyer vers des descriptions homogènes de leur contenu précis et de leurs métadonnées. Des normes d'interopérabilité sont donc attendues pour rendre possible une meilleure exploitation des nombreuses données de santé collectées.
· Deuxième frein : la durée et la complexité des procédures réglementaires d'accès. Il existe certes des procédures d'accès simplifiées, sur déclaration, qui permettent de disposer de certaines données du SNDS sans avis de la Cnil (ces procédures représentent désormais 72 % des accès), en respectant des méthodes simplifiées. Depuis 2015, la Cnil a ainsi établi 13 référentiels permettant la mise en oeuvre de traitements de données de santé sur la base d'une simple déclaration de conformité. Dans les autres cas, l'accès aux données fait l'objet d'un avis du Comité éthique et scientifique pour les recherches, les études et les évaluations dans le domaine de la santé (Cesrees), rendu dans un délai de 1 mois (renouvelable une fois), avant décision de la Cnil, qui dispose de 2 mois (délai renouvelable une fois).
· À ces délais réglementaires s'ajoutent des délais d'accès contractuels et techniques. Ainsi, le rapport Marchand-Arvier note que le délai effectif de mise à disposition concrète des données du SNDS après autorisation s'élève à 10 à 12 mois et s'est allongé entre 2020 et 2022. Les startups se plaignent régulièrement des difficultés et de la longueur des négociations avec les producteurs de données. Il est souvent difficile de s'accorder sur le partage de la valeur apportée par l'utilisation des données.
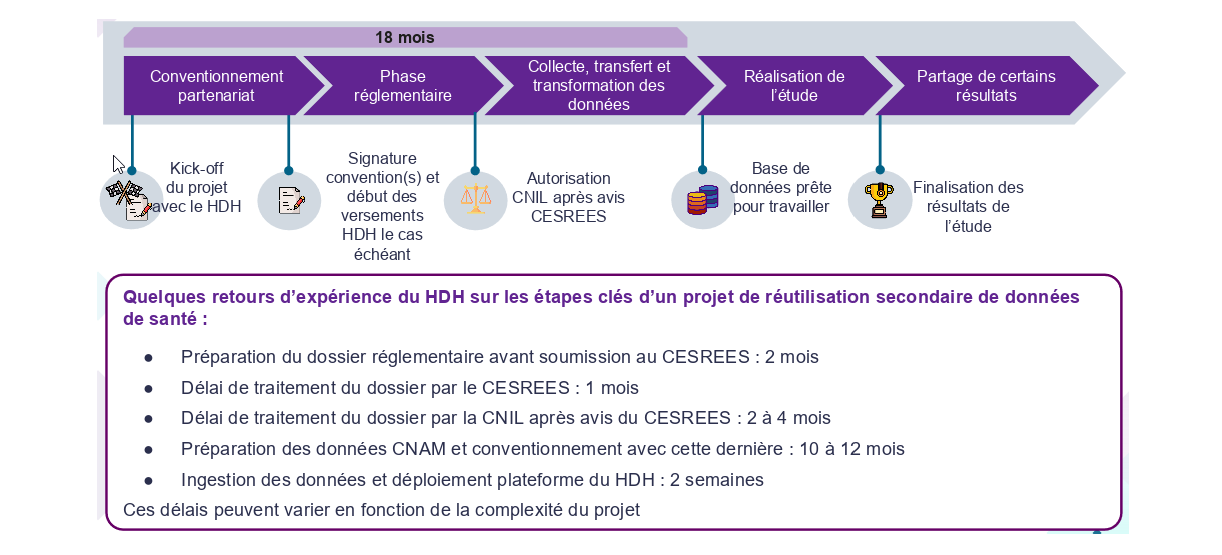
Au final, on constate en France un délai moyen de 18 mois entre le lancement d'un projet de recherche et l'accès effectif aux données de santé, alors que dans d'autres pays comme les États-Unis, Israël ou Singapour les délais sont bien plus courts.
Les grandes étapes d'un projet de recherche à partir de données de santé en France
Source : Rapport Marchand-Arvier (d'après les chiffres du HDH)
Afin de faciliter l'accès aux données de santé pour des projets d'intérêt public, notamment pour la recherche et la construction d'algorithmes médicaux et lever ces différents freins, la France s'est dotée depuis la fin 2019, d'une plateforme des données de santé (PDS), appelée Health Data Hub (HDH). Le HDH est désormais le guichet unique d'accès aux données de santé et a un rôle de facilitateur pour les porteurs de projets. En quatre ans, le HDH a accompagné un peu plus de 100 projets.
Source : Health Data Hub
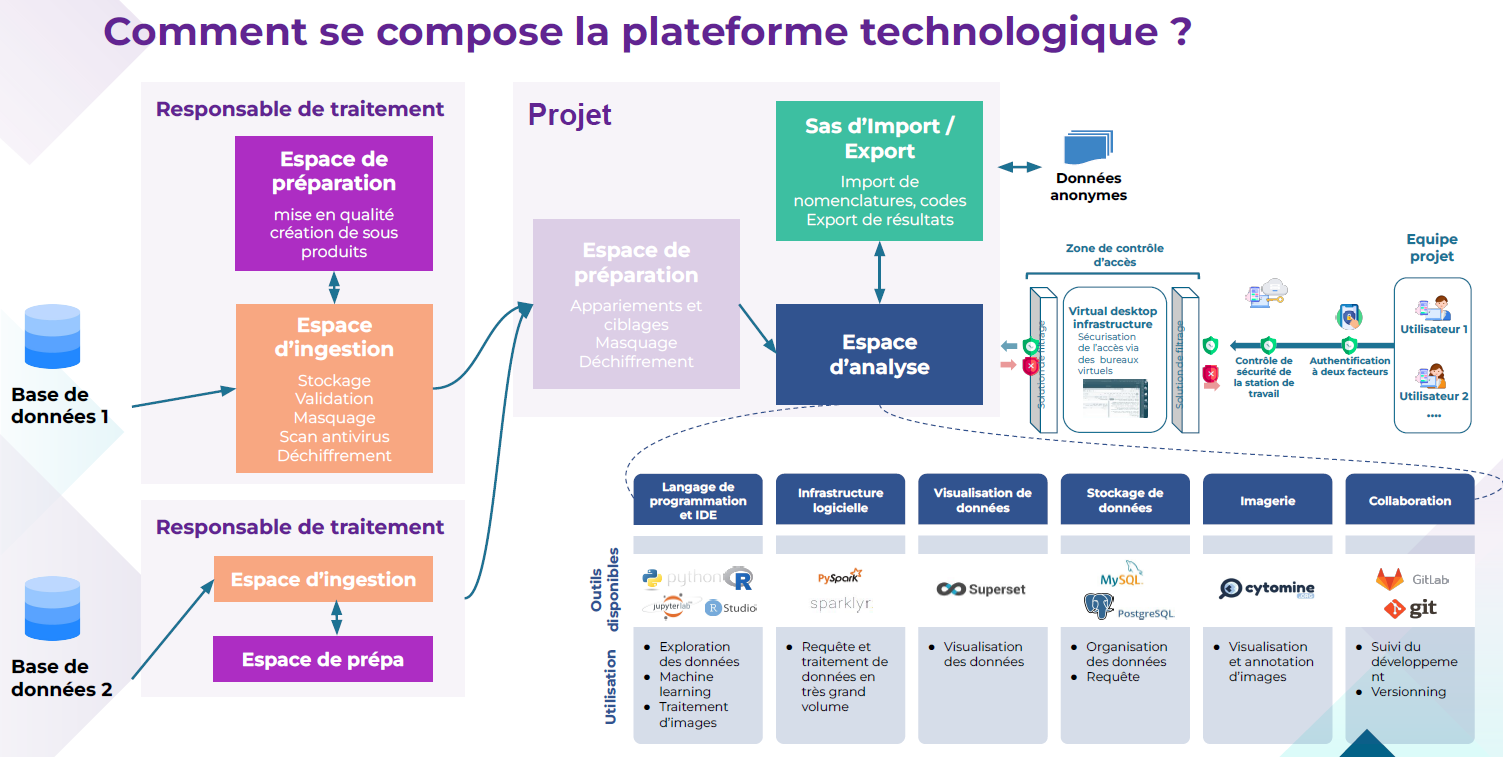
Lors de son audition, le HDH a insisté sur le caractère incontournable des données dans toute stratégie d'IA. Il s'agit à la fois de repérer les données accessibles (catalogue), au-delà du seul SNDS, de qualifier les bases de données et ensuite de les utiliser de manière sécurisée.
Le HDH met en oeuvre une plateforme technologique complexe (voir schéma) qui assure l'ingestion des données pseudonymisées, le stockage des bases de données, la mise à disposition de données dans des espaces d'analyse, enfin l'accès à des outils d'exploitation de données.
Source : Health Data Hub
La question sensible de l'hébergement des données de santé par le HDH
L'hébergement des données du SNDS gérées par le HDH a donné lieu à un débat autant technique que politique. Seul acteur certifié pour l'hébergement des données de santé, la société Microsoft Azure a été désignée en 2019 pour fournir ce service au HDH.
Or, les sociétés américaines étant soumises au Cloud Act ainsi qu'à diverses dispositions d'application extraterritoriale, la possibilité de voir les données de santé des patients français accessibles par les pouvoirs publics américains a fortement ému. Les protections juridiques apportées par les textes régissant les transferts de données entre Europe et États-Unis et le fait que les données resteront hébergées par Microsoft Azure sur des serveurs situés physiquement sur le territoire français n'ont pas levé toutes les craintes.
La constitution d'une solution de cloud souverain sécurisée (SecNumCloud) et surtout suffisamment performante pour héberger les données du SNDS est donc en cours, mais ne devrait pas voir le jour avant la fin 2025.
Validé par la Cnil début 2024 pour une durée de 3 ans, l'hébergement par la même société Microsoft Azure de l'entrepôt de données de santé EMC2 souhaité par l'Agence européenne du médicament (EMA) et géré lui aussi par le HDH s'est effectué à partir du même constat de l'incapacité d'une offre souveraine à offrir des services techniquement satisfaisants. Ce choix a suscité les mêmes critiques.
L'orientation politique vers un cloud souverain sécurisé ne doit pas être remise en cause, car un certain degré de maîtrise technologique est la condition pour ne pas dépendre d'acteurs hors UE.
B. LA BONNE UTILISATION DES DONNÉES ET LA LUTTE CONTRE LES BIAIS
Si l'accès aux données est stratégique, leur bonne utilisation pour entraîner les systèmes d'IA l'est tout autant. Avec le développement des IA génératives, fondées sur de l'apprentissage automatique, la lutte contre les biais doit être intégrée au processus de production d'information par le système lui-même.
Ainsi, l'entraînement des IA génératives sur des données non représentatives de la population générale par manque de diversité d'âge, de genre, voire d'origine ethnique dans les données de base, peut conduire à « passer à côté » lorsque l'on cherche à appliquer l'outil sur des individus présentant des caractéristiques spécifiques. En imagerie médicale, par exemple, si une base comprend plus d'hommes que de femmes, ces dernières risquent d'être moins bien diagnostiquées par l'IA35(*).
Une récente revue de littérature a identifié six sources de biais inhérents aux données numériques de santé : des biais liés aux essais cliniques antérieurs, des biais liés à l'insuffisance de données ou leur insuffisante annotation, des biais liés à des préjugés cliniques, des biais de références, des biais liés aux profils de risques, et des biais liés aux machines et algorithmes eux-mêmes36(*). Ces multiples biais peuvent se combiner entre eux et avoir des effets exponentiels.
Si les professionnels de santé utilisateurs des systèmes d'IA ne connaissent pas bien les limites de leurs outils, et notamment ne sont pas informés des possibles biais des systèmes d'IA qu'ils utilisent, ils ne peuvent pas se distancier des résultats proposés par les machines et sont alors susceptibles d'être induits en erreur dans leur analyse clinique.
Il existe également un risque d'erreurs non détectées lorsque l'IA travaille sur des données « falsifiées » (volontairement ou pas), conduisant à des résultats absurdes qu'une intelligence humaine aurait pu écarter par un simple raisonnement logique. Il est donc nécessaire d'effectuer un contrôle sur les données qui seront utilisées dans les systèmes d'IA en santé.
II. FAIRE FACE À LA CRAINTE D'UNE MÉCANISATION DE LA MÉDECINE
A. LE SCÉNARIO REDOUTÉ DU ROBOT-MÉDECIN
Dès lors que les performances des IA se rapprochent de celles des médecins, ce qui est déjà le cas en analyse d'images, se pose la question du remplacement à terme de l'homme par la machine. Il est évident que les systèmes d'IA n'ont aujourd'hui pas la capacité à assurer une analyse complète des besoins du patient et n'interviennent que pour répondre à une question précise : localisation de tumeurs, identification de biomarqueurs, mise en forme d'informations médicales dispersées, etc. Une IA globale capable de prendre en charge un patient paraît à ce stade hors d'atteinte.
Mais l'expérience de la performance d'IA peut conduire à une automatisation de nombreuses tâches d'analyses complexes, contribuant à créer une nouvelle expertise de la machine, à laquelle on sera enclin à faire systématiquement confiance dès lors que l'on constate qu'elle se trompe rarement. Lors de son audition, le Pr Guillaume Assié soulignait que l'aide au diagnostic, lorsqu'elle fonctionne bien, pouvait rapidement se transformer en diagnostic automatisé. Avec l'automatisation, il existe un risque réel de déqualification de praticiens amenés à ne plus réaliser certains actes. L'expertise humaine sera transférée à un petit nombre d'hyper-spécialistes de l'ingénierie biomédicale numérique qui auront la lourde charge de qualifier les systèmes d'IA et de les surveiller.
L'intégration d'IA performantes dans les processus de soins pourrait conduire à une standardisation des procédures médicales, une meilleure application des protocoles de soins ou des bonnes pratiques correspondant au dernier état de la science. Il pourrait en résulter un bénéfice global pour les patients, avec une limitation des erreurs médicales et davantage d'égalité dans la qualité des prises en charge.
Pour autant, une confiance aveugle dans l'IA pourrait aussi amener à rater les cas particuliers, ou à ne pas pouvoir traiter des maladies émergentes, non répertoriées. L'entraînement des IA peut au demeurant avoir tendance à stériliser l'innovation. Dans son rapport à l'Académie nationale de médecine sur les IA génératives, le Pr Bernard Nordlinger note que « l'analyse rétrospective, si elle contribue à construire une base de travail ne peut suffire à générer des hypothèses originales, par essence prospectives et issues de la créativité et de l'inventivité du chercheur ».
Un autre souci connu est la propension des IA génératives, qui fonctionnent sur des modèles probabilistes, à produire des « hallucinations », c'est-à-dire des réponses fausses, certes rares, mais d'autant plus problématiques qu'elles peuvent être non détectables (voir rapport thématique n° 1 p. 23).
Le corollaire de cette évolution serait un déplacement de responsabilité du praticien vers le fournisseur de la solution informatique : la non-détection d'une tumeur par la machine ne pourrait pas être reprochée au radiologue, dès lors que l'analyse des clichés radiologiques est faite de manière automatique.
Le médecin serait alors réduit à un rôle de supervision et éventuellement de sélection des IA qu'il envisage d'utiliser pour son travail. Outre les difficultés techniques qu'il rencontre, la prise en charge médicale ne se résumant pas à une suite d'équations à résoudre et l'IA n'ayant pas une capacité globale d'analyse, ce scénario se heurte à de réels obstacles en termes d'acceptabilité sociale et éthique. Il est ainsi établi qu'on accepte moins bien les erreurs faites par des machines que celles faites par des humains. Le chemin vers une IA de confiance ne se confond pas avec une IA totalement autonome et une approche mécaniste de la santé.
B. LE SCÉNARIO PRÉFÉRÉ DU SOIGNANT AUGMENTÉ
Un autre scénario, plus satisfaisant mais aussi plus probable, est celui du soignant augmenté. L'IA constituerait un outillage supplémentaire. Le Pr Alexandre Loupy rappelait, lors de son audition, que les médecins n'ont jamais cessé d'inventer des outils pour améliorer leur pratique : stéthoscope, électrocardiogramme, radiographies. L'IA est un outil supplémentaire de connaissance, une sorte de « cognoscope » capable de faire des synthèses que l'on ne peut plus faire nous-mêmes du fait du trop-plein d'informations.
Mais comme le faisait remarquer le Pr Bernard Nordlinger, les outils d'IA proposant de faire une synthèse diagnostique complète n'ont pas encore fait leurs preuves. Les soignants conservent donc toute leur place pour rassembler les informations venant de sources disparates. Par ailleurs, la relation entre un médecin et un patient reste incontournable pour collecter des informations importantes qui peuvent être hors du champ de vision d'une IA.
Pour que l'utilisation de l'IA comme outil contribue à l'amélioration de la santé, il est important que ses mécanismes soient compris par l'ensemble des parties prenantes, médecins comme patients. L'explicabilité constitue un impératif éthique qui va au-delà de la simple exigence de transparence algorithmique. Il ne s'agit pas d'atteindre une explicabilité complète, d'ailleurs inatteignable avec les technologies d'IA génératives du fait de leur fonctionnement même, mais de comprendre la manière dont les IA déployées parviennent à fournir des résultats. L'enjeu est de pouvoir connaître les biais possibles, écarter les résultats douteux, garder une distance critique, pour que l'IA reste au final un outil au service d'une prise de décision demeurant dans les mains des médecins.
L'explicabilité est importante pour les soignants, mais elle l'est aussi pour les patients qui doivent pouvoir effectuer des choix éclairés sur leur prise en charge.
Cette exigence d'explicabilité vaut dans les activités cliniques, mais aussi dans le domaine de la recherche. Ainsi, en recherche, les IA génératives sont capables de produire des synthèses mais ne peuvent pas fournir une bibliographie expliquant d'où elles tirent leurs informations. Pire, lors de son audition, la Pr Brigitte Seroussi indiquait qu'une IA pourrait être trompée par de fausses publications, sans avoir les moyens de repérer que les données d'entrée posent problème. Lors de la crise du covid, plusieurs publications erronées ont été publiées dans des revues scientifiques avant d'être retirées. Même des éditeurs de référence comme The Lancet ont été touchés.
Dans ces conditions, il serait dangereux de faire du soignant un simple opérateur de l'IA, dépourvu de capacités de contrôle et n'exerçant plus que formellement sa fonction de décision. À l'inverse, le soignant augmenté de demain aura besoin d'outils d'IA qui l'aident dans sa pratique, lui permettent de gagner du temps, de disposer d'informations plus complètes et fiables pour poser les meilleurs diagnostics et proposer les meilleurs traitements à chaque patient.
III. SE METTRE EN ORDRE DE BATAILLE POUR TIRER LE MEILLEUR PARTI DE L'IA POUR NOTRE SYSTÈME DE SANTÉ
A. DONNER UN CADRE ÉTHIQUE SOLIDE À L'IA EN SANTÉ
Les pratiques médicales doivent être conformes à l'éthique. Celle-ci implique un certain nombre de comportements vertueux qui reposent sur quelques principes solides : ceux du code de Nuremberg de 1947 (impliquant par exemple le consentement libre et éclairé des individus dans le cadre de la recherche médicale), de la déclaration d'Helsinki de 1964 ou encore de la Convention d'Oviedo de 1997.
Quatre principes constituent le socle de la bioéthique : le respect de l'autonomie de la personne, la bienfaisance, la non-malfaisance et la justice (principes énoncés par le rapport Belmont de 1979). Le développement du numérique dans le domaine de la santé transforme les conditions d'exercice de l'éthique médicale et l'IA ajoute une complexité supplémentaire.
À l'échelle internationale, l'OMS a publié en 2021 des lignes directrices pour l'éthique et la gouvernance de l'IA pour la santé37(*), complétées en 2024 par des lignes directrices pour l'éthique et la gouvernance des grands modèles multimodaux38(*) qui fixent quelques grands principes.
Les 6 principes éthiques régissant l'utilisation de l'intelligence artificielle pour la santé d'après l'OMS
· Protéger l'autonomie de l'être humain : la décision médicale ne peut être totalement déléguée à la machine ;
· Promouvoir le bien-être et la sécurité des personnes et l'intérêt public : les IA ne doivent pas pouvoir nuire ;
· Garantir la transparence, l'explicabilité et l'intelligibilité des IA ;
· Favoriser la responsabilité et la responsabilisation : l'IA ne doit pas conduire à exonérer les humains de leurs responsabilités ;
· Garantir l'inclusion et l'équité : l'IA ne doit pas être discriminatoire et corriger les biais ;
· Promouvoir une IA réactive et durable (en limitant son impact environnemental).
Dans ses lignes directrices de 2024, l'OMS indique que les grands modèles multimodaux (LMM) de l'IA générative font peser des risques supplémentaires (augmentation des biais d'automatisation) qui nécessitent de renforcer les exigences éthiques par un renforcement des audits des outils d'IA et une évaluation plus approfondie des résultats.
À l'échelle nationale, un corpus éthique sur l'IA en santé est aussi en cours de construction. Créé en 1983, le Comité consultatif national d'éthique (CCNE) formule des avis qui constituent autant de lignes directrices que l'ensemble des acteurs du secteur médical et biomédical (chercheurs, médecins, ingénieurs) doivent s'efforcer de mettre en oeuvre. Il a créé en son sein en 2019 un Comité national pilote d'éthique du numérique (CNPEN) pour aborder de manière globale les enjeux d'éthique du numérique.
Les IA ne répondent pas à des impératifs moraux. Ce sont des outils dotés d'une certaine autonomie de fonctionnement mais sans conscience et sans affect. Toutefois, les concepteurs de ces IA peuvent les doter de filtres permettant de respecter certaines prescriptions morales. Par ailleurs, la manière de se servir des IA n'est pas neutre et les données manipulées, touchant à la santé des individus et à leur vie privée, sont sensibles.
Le CNPEN a déjà formulé plusieurs avis sur les utilisations de l'IA en santé39(*) et un avis commun au CCNE et au CNPEN est en préparation sur l'IA dans le diagnostic médical. L'acceptabilité sociale de l'IA en santé passe en effet par le respect de règles éthiques garantissant une certaine morale de l'IA.
Ainsi, les fournisseurs de solutions d'IA sont incités à former les utilisateurs, leur décrire les possibles biais, leur fournir une documentation claire et les informer des effets d'éventuelles mises à jour. De leur côté, les utilisateurs de l'IA doivent informer les patients des méthodes qu'ils utilisent pour formuler un diagnostic. L'utilisation de l'IA ne doit pas être cachée et l'IA ne doit pas constituer une « boîte noire » incompréhensible.
Un autre principe éthique impose que les responsabilités du fournisseur d'IA et de son utilisateur soient bien définies. Ce dernier doit disposer également d'outils de contrôle. La décision finale ne doit pas lui échapper.
Une autre exigence tient au consentement des patients et à la protection de leur vie privée : la collecte des données doit avoir été acceptée et ces dernières doivent être anonymisées. Seules les données nécessaires au traitement doivent être collectées.
Le développement de l'IA conduit à devoir adapter le cadre juridique de la collecte et du traitement des données ainsi que des usages qui en découlent. Le cadre de la protection des données personnelles régi par la loi de 1978 et mis en oeuvre par la Cnil doit ainsi évoluer. À l'échelle européenne, la conciliation entre une exigence forte de protection des droits et de soutien à l'innovation s'est concrétisée dans la « loi européenne sur l'intelligence artificielle » dite AI Act. Ce texte, formellement adopté en mars 2024, impose que les produits, services et procédés mis sur le marché européen respectent une série d'exigences : non-discrimination dans la construction des algorithmes, sécurité informatique, garantie d'un contrôle humain, information et transparence, marquage CE mais aussi durabilité environnementale.
L'AI Act : un règlement européen pour concilier innovation et protection
Le règlement européen sur l'IA définit différents niveaux de risques :
· les systèmes d'IA à risque inacceptable sont interdits : il s'agit par exemple des systèmes de notation sociale ou des IA manipulatrices (techniques subliminales, exploitation de vulnérabilités, systèmes de notation sociale) ;
· les systèmes d'IA à haut risque (dont la liste est établie à l'annexe III du règlement) sont fortement réglementés : leurs fournisseurs doivent informer de la manière dont ils collectent et traitent les données, garantir la cybersécurité de leur dispositif, prendre des précautions dans la gestion de leurs données ;
· les systèmes d'IA à risque limité sont soumis à des obligations légères de transparence ;
· les systèmes d'IA considérés comme sans risque ne sont soumis à aucune obligation.
Les IA organisant l'accès aux soins de santé sont considérées comme à haut risque. Néanmoins, les outils construits pour la recherche sont hors du champ d'application du règlement. Par ailleurs, son article 59 prévoit que les données à caractère personnel collectées légalement peuvent être utilisées pour entraîner des algorithmes en mode dit « bac à sable » pour la détection, le diagnostic, la prévention, le contrôle et le traitement des maladies ainsi que l'amélioration des systèmes de soins de santé.
Le projet de règlement européen prévoyant la mise en place d'un espace européen des données de santé (EEDS), en cours d'adoption, normalise les possibilités de recueil des données de santé, de partage et de traitement de celles-ci, pour concilier là aussi l'exigence de protection des données personnelles et l'impératif d'utilisation des données disponibles sur la santé pour améliorer globalement la prise en charge des patients.
B. APPORTER UN SOUTIEN PUBLIC FORT AU DÉPLOIEMENT DE L'IA EN SANTÉ
Il existe aujourd'hui un foisonnement d'initiatives pour déployer des IA dans le secteur de la santé, avec des technologies très variées : apprentissage machine, apprentissage profond, réseaux de neurones. Nous en sommes à un stade encore largement expérimental, fait de tâtonnements et d'ajustements, mais aussi de changements rapides.
Le rejet de ces nouvelles techniques n'est une option ni réaliste ni juste. Il est évident que des outils efficaces seront adoptés par les médecins et les patients. Il ne serait par ailleurs pas éthique de refuser d'utiliser l'IA si celle-ci permet de « mieux soigner ».
Les domaines des applications numériques de santé recensées par France Biotech sont très divers et cet outillage supplémentaire devrait se révéler globalement utile.
Annoncée en 2018 à la suite du rapport Villani, la stratégie nationale pour l'intelligence artificielle (SNIA) visait à positionner la France comme un des leaders européens et mondiaux de l'IA et s'appuyait sur les financements du plan France 2030. La santé constitue l'un des volets importants de cette stratégie.
Sur le plan du pilotage et de la gouvernance, la France s'est ainsi dotée en 2019 (stratégie Ma Santé 2022) d'une Délégation au numérique en santé (DNS) devenue direction d'administration centrale du ministère de la santé en mai 2023, ainsi que d'une Agence de l'innovation en santé (AIS), créée en 2022 et chargée notamment de suivre le volet santé de France 2030 (environ 10 % de l'enveloppe globale des 54 milliards d'euros du plan) ainsi que de faciliter les démarches des porteurs de projets. Lors de son audition, l'AIS a précisé accompagner aujourd'hui une quarantaine de projets innovants en santé, parmi lesquels la moitié utilisent des technologies d'IA.
L'objectif consiste à tirer parti des innovations pour améliorer la santé, mais aussi à se doter d'un tissu économique capable de porter ces innovations. Il s'agit de tirer parti de l'excellence de nos laboratoires et de nos chercheurs en santé et biotechnologies pour développer les pépites technologiques de demain et ne pas voir fuir la valeur créée aux États-Unis ou en Chine.
Le rapport de mars 2024 de la Commission de l'intelligence artificielle40(*), présidée par Philippe Aghion et Anne Bouverot, entendus par la délégation à la prospective du Sénat le 26 mars 202441(*), pointe bien cette difficulté en indiquant que « la France et l'Europe encourent le risque d'un rapide déclassement économique », ajoutant que « le retard en matière d'intelligence artificielle porte atteinte à notre souveraineté. Une faible maîtrise de la technologie implique effectivement un lien à sens unique vis-à-vis des autres pays. »
Le développement de solutions numériques en santé exploitant le potentiel de l'IA est un axe majeur pour les entreprises du secteur de la santé, mais il se heurte aux difficultés de financement, au moins dans les premières phases de tests et de montée en puissance.
Des financements privés sont mobilisés à travers les levées de fonds opérées par les sociétés de la « healthtech ». En Europe et aux États-Unis, celles-ci ont atteint plus de 55 milliards d'euros en 2021 (dont les 2/3 par des sociétés américaines) ; ce chiffre est retombé à 29,5 milliards d'euros en 2022 et 23,7 milliards d'euros en 2023. En France, on est passé de 2,6 milliards d'euros en 2022 à 1,76 milliard d'euros en 2023, d'après le panorama 2024 dressé par France Biotech, l'association fédérant les entreprises du secteur de la santé.
Des soutiens publics sont donc également nécessaires pour suppléer ou compléter un financement privé insuffisant. D'après l'AIS, la stratégie d'accélération santé numérique (SASN) a permis de soutenir en deux ans 148 projets pour 320 millions d'euros d'aides. Les financements publics favorisant l'IA en santé peuvent s'appuyer notamment sur le programme d'équipement prioritaire de recherche (PEPR) Santé numérique doté de 60 millions d'euros, le financement des entrepôts de données de santé pour 75 millions d'euros, l'appel à manifestation d'intérêt « compétences et métiers d'avenir » pour 10 millions d'euros, le grand défi IA doté de 30 millions d'euros sur le volet santé ou encore le projet important d'intérêt commun européen commun (PIIEC) doté de 80 millions d'euros. L'AIS estime le montant total d'investissements publics dans l'IA en santé à environ 400 millions d'euros depuis le lancement des programmes d'investissement d'avenir (PIA).
Un exemple de projet soutenu : MediTwin
Annoncé fin 2023, le projet MediTwin vise à développer une plateforme européenne et souveraine de services pour l'aide à la décision médicale. Il regroupe 13 partenaires (1 industriel : Dassault Systèmes, 3 startups, 1 organisme de recherche, 7 IHU et 1 CHU).
Il repose sur la virtualisation des organes et des systèmes physio-pathologiques à partir des données médicales pour une amélioration de l'efficience des soins ainsi que de l'efficacité et la sécurité des pratiques médicales, reposant sur la capacité à prédire l'évolution et le succès des différentes interventions possibles.
Dans le cadre du projet, sept cas d'usage seront développés dans différentes pathologies (notamment en oncologie, neurologie dont Alzheimer, cardio-vasculaire) pour permettre aux spécialistes de partager les données sur les patients, d'apporter une réponse à la fragmentation actuelle des connaissances ainsi que des savoir-faire complexes, d'améliorer l'accès et l'égalité aux soins des patients, sans oublier d'améliorer aussi les conditions de travail du personnel soignant.
Dans le cadre de France 2030, MediTwin bénéficiera de 2024 à 2029 d'un financement public représentant un levier fort pour soutenir le développement de la filière santé numérique, avec l'objectif de transformer un marché intérieur français en un secteur économique exportateur et innovant.
Source : Agence de l'innovation en santé
CONCLUSIONS ET RECOMMANDATIONS
Confronté à l'explosion des données, à la complexité des situations, dans un contexte de tensions budgétaires et de temps contraint pour assurer les soins aux patients, le secteur de la santé est l'un de ceux qui pourraient le plus tirer parti des progrès de l'IA.
Le potentiel de transformation des pratiques soignantes par l'IA, au bénéfice des patients, est fort. Le caractère spectaculaire de l'IA générative a porté un regain d'engouement pour l'IA, même si nombre des applications de l'IA en santé ne relèvent pas de l'IA générative mais de l'IA classique.
Il n'y a pas un modèle unifié d'IA mais en réalité plusieurs formes d'IA, pour lesquelles une première exigence réside dans la qualité des données d'entrée utilisées pour entraîner les modèles d'apprentissage automatisé et d'apprentissage profond. Les utilisations de l'IA en santé sont également très variées : recherche, dépistage, fourniture d'informations, aide à la décision, production documentaire.
La médecine a toujours intégré les meilleures connaissances et l'ensemble des technologies disponibles pour améliorer la prise en charge des patients. Si l'IA est capable de résoudre des questions pratiques comme la lecture d'un cliché radiologique, la synthèse d'articles scientifiques ou la modélisation 3D de protéines, elle sera à n'en pas douter adoptée par ceux dont le travail quotidien sera ainsi facilité.
Mais cette adoption pourrait se faire à un rythme variable : certains y auront accès plus vite que d'autres, certains verrous psychologiques ou financiers créeront des réticences. Les inégalités de santé pourraient s'accroître si l'on n'y prend pas garde.
L'IA va aussi transformer la relation entre patients et médecins, comme l'a déjà fait la démocratisation de l'information médicale grâce à Internet. Mieux informés, les patients seront plus exigeants mais ils pourront aussi être davantage acteurs des soins.
Enfin, l'IA pourrait transformer l'approche du soin, fondée largement aujourd'hui sur le curatif. Avec l'IA et le développement des dépistages et prédictions à partir de données massives, c'est vers une médecine plus personnalisée et plus axée sur la prévention de l'apparition de potentielles maladies que l'on s'orientera. Nous pourrions faire ainsi des économies dans les dépenses de santé, en évitant des traitements curatifs coûteux. Mais nous pourrions aussi multiplier les examens de contrôle et dériver vers un monitoring permanent anxiogène.
L'économie de la santé et celle du numérique seront davantage imbriquées, et l'enjeu d'une IA souveraine n'est pas à négliger dans les politiques publiques nationale et européenne.
Quatre axes se dégagent aujourd'hui pour une IA en santé efficace et juste.
4 AXES POUR UNE IA EN SANTÉ EFFICACE ET JUSTE
I. DÉVELOPPER UNE CULTURE DE L'IA EN SANTÉ PAR LA FORMATION INITIALE ET CONTINUE DES SOIGNANTS
Comme toute nouvelle technologie, son bon usage, voire son usage tout court, passe par une étape de prise en main par ses utilisateurs et ses bénéficiaires.
Si l'informatique contemporaine se caractérise par d'importants efforts de fluidité et le souci du caractère très intuitif des interfaces homme-machine, le fonctionnement de l'IA dans la santé doit être bien compris afin d'en tirer profit, mais aussi d'en mesurer les limites. La formation à l'IA devrait donc être intégrée aux cursus universitaires pour les médecins mais aussi les professions paramédicales.
Pour adapter les personnels de santé déjà en poste, des efforts renforcés de formation continue à l'utilisation des outils d'IA devraient aussi être envisagés.
Enfin, un nouveau métier d'opérateur de l'IA en santé pourrait voir le jour, pour gérer la complexité et assurer une médiation entre les différents acteurs du système de santé : soignants, patients et producteurs de dispositifs médicaux numériques.
II. ACCÉLÉRER L'ACCÈS DES CHERCHEURS ET DES STARTUPS AUX DONNÉES SECONDAIRES DE SANTÉ
L'accès aux données est une condition indispensable pour pouvoir développer des solutions de haut niveau fondées sur l'utilisation de l'IA. Cela est possible sans remise en cause fondamentale des grands principes de protection des données personnelles, en développant les méthodologies de référence (MR) dont le respect permet de se passer des procédures d'autorisation plus lourdes.
Une part importante des délais d'accès ne résulte pas de verrous juridiques mais de contraintes techniques. Il convient de faire adopter par le plus grand nombre de producteurs de données de santé des normes d'interopérabilité facilitant les croisements, et de renforcer le rôle du Health Data Hub comme fédérateur des différentes bases de données.
Enfin, des contrats types pourraient lever les verrous contractuels entre producteurs et utilisateurs de données, en définissant des normes de partage de la valeur.
III. CONSTRUIRE UN CADRE ÉTHIQUE ROBUSTE DE L'INTELLIGENCE ARTIFICIELLE EN SANTÉ
La confiance dans l'IA de la part de l'ensemble des acteurs de la santé, patients comme professionnels, est conditionnée au respect de principes éthiques garantissant le caractère fiable et non discriminant du fonctionnement des IA mises à disposition pour notre santé, la protection des données personnelles de santé, qui sont des données sensibles qu'on ne souhaite pas voir être exposées sur la place publique, ou encore l'absence de délégation complète de la prise de décisions importantes à la machine. Patients comme soignants doivent pouvoir comprendre avec précision la portée et les limites de l'utilisation des solutions d'IA disponibles.
Les exigences éthiques doivent être intégrées dans les dispositifs d'IA dès leur conception (ethics by design) et les enjeux d'éthique doivent être intégrés eux aussi dans la formation des soignants à l'IA.
Enfin, les exigences éthiques doivent trouver leur traduction juridique dans les textes et leur mise en application concrète. Le caractère dissuasif des sanctions prévues par l'AI Act européen en cas de manquement des fournisseurs de services numériques à risque élevé à leurs obligations (amende de 35 millions d'euros ou 7 % du chiffre d'affaires) constitue une forte incitation à placer la barre haut en matière d'éthique. Il conviendra toutefois que les instances nationales de contrôle (en France, la Cnil) disposent de moyens renforcés d'investigation et d'expertise pour que la menace de sanctions puisse jouer à plein.
IV. ÊTRE CAPABLE DE FINANCER LA « COURSE À L'IA »
Dans le domaine de la santé comme dans les autres domaines, l'IA connaît un essor qui se traduit par la multiplication d'initiatives et d'expérimentations. L'irruption de l'IA générative a donné un coup d'accélérateur aux investissements et contribue à faire évoluer très vite les technologies et leurs possibilités d'application.
Cette phase expérimentale un peu foisonnante qui repose sur une multitude d'acteurs pourrait être suivie d'une phase de stabilisation qui ne laissera que quelques opérateurs sur le marché. Le rapport de la Commission de l'intelligence artificielle de mars 2024 alerte sur le risque de rater la marche et de dépendre in fine de firmes américaines ou chinoises. Pour éviter un décrochage français et européen, il propose d'investir 5 milliards d'euros sur 5 ans. Il convient qu'une part significative de cette enveloppe soit orientée sur l'IA dans le domaine de la santé.
L'ambition d'un écosystème de l'IA en santé peu dépendant de partenaires étrangers passe aussi par l'accélération du projet de cloud sécurisé souverain, car nos données de santé, au même titre que nos données de sécurité ou nos données fiscales, ne sauraient être soumises au risque de transmission à une puissance étrangère.
Enfin, la course à l'IA ne trouvera un aboutissement concret pour les patients que si, au-delà des investissements initiaux, un modèle économique est trouvé pour financer les nouveaux outils par une tarification adaptée. Il s'agit de disposer de fonds au-delà de la seule phase de mise en route. De ce point de vue, une enveloppe dédiée au secteur hospitalier pourrait, sur le modèle du financement des missions d'intérêt général, favoriser l'acquisition et la maintenance de solutions logicielles performantes.
EXAMEN EN DÉLÉGATION
Réunie le mardi 21 mai 2024, la délégation à la prospective a examiné le rapport de Mme Anne Ventalon et M. Christian Redon-Sarrazy sur « IA et santé ».
Mme Christine Lavarde, présidente. - Bonjour à tous et merci de vous être libérés pour cet horaire inhabituel qui nous permet de concilier au mieux les contraintes d'agenda des membres de la délégation. Le rapport sur IA et santé que nous allons examiner dans un instant est attendu. Pas plus tard encore que ce matin, le précédent rapport de la délégation a été cité dans un colloque autour de l'intelligence artificielle. Il a notamment été souligné le côté très didactique de la présentation qui en fait un document agréable à lire sur un sujet qui n'est pas forcément toujours accessible. Nos travaux sont connus. J'en veux pour preuve l'invitation que j'ai reçue en tant que présidente de la délégation pour un événement qui se tient aujourd'hui à l'Élysée autour de l'intelligence artificielle.
Je ne vais pas être plus longue et laisser les rapporteurs présenter leurs travaux. Pour avoir parcouru hier soir leur rapport, je pense qu'il est vraiment dans la continuité de ce qui a été réalisé sur IA et services financiers et sociaux, c'est-à-dire qu'il présente un bon équilibre entre les opportunités de l'IA, qui sont réelles, et en même temps les zones d'ombres ou de risques sur lesquelles il faut se préparer pour disposer à la fin d'une intelligence artificielle responsable, dans une définition très large du terme responsable.
Mme Anne Ventalon, rapporteure. - Merci madame la Présidente. Après la présentation par nos collègues Sylvie Vermeillet et Didier Rimbaud, du premier rapport thématique de la délégation sur l'intelligence artificielle consacré aux impôts, prestations sociales et à la lutte contre la fraude, nous avons le plaisir avec Christian Redon-Sarrazy, de vous présenter le deuxième rapport thématique portant sur l'intelligence artificielle et la santé.
Pour disposer d'un panorama pertinent et fiable sur le sujet, nous avons procédé, entre le 30 janvier et le 19 mars dernier, à 15 auditions et nous avons aussi reçu quelques contributions écrites complémentaires. Nous avons également participé à la table ronde organisée par la commission des affaires sociales du Sénat sur le sujet de l'intelligence artificielle en santé le 13 mars dernier. Tous ces échanges nous ont confirmé le grand intérêt pour l'IA de l'ensemble des acteurs du monde de la santé : médecins, chercheurs, entreprises du numérique en santé, pouvoirs publics. Et en même temps, l'intelligence artificielle n'est pas encore totalement rentrée dans les habitudes et continue à susciter interrogations, voire controverses.
Sans prétendre à lever tous les doutes ou à figer la réflexion, notre rapport vise simplement à faire un état des lieux et à émettre quelques recommandations afin que notre système de santé et notre pays ne ratent pas le virage de l'IA, et tire aussi le maximum de bénéfices de cette technologie pour les patients, pour les professionnels de santé et plus globalement, pour l'organisation de notre système de soins.
Notre premier constat est que la santé est un bon terrain de jeu pour déployer les technologies d'intelligence artificielle, et ce, pour une raison simple : la prise en charge de la santé passe par le traitement de masses de plus en plus importantes et diversifiées de données. Il est de moins en moins possible pour le cerveau humain de gérer autant de données dans des délais très courts. Les outils numériques sont donc nécessaires pour l'aider. La mise à disposition de l'information médicale par Internet et par des bases de connaissances de plus en plus complètes et facilement accessibles constitue un premier levier d'aide, au demeurant, largement accessible au grand public. Un deuxième levier réside dans les systèmes numériques d'aide à la décision, par exemple pour l'interprétation des clichés radiologiques, pour celle des analyses biologiques ou encore pour la prescription de médicaments. Dans le domaine médical, l'IA intervient pour automatiser le traitement de nombreuses données et pour en faire quelque chose d'utile dans le processus de soin.
À ce stade, on peut rappeler la définition très large donnée à l'IA par l'article 3 du règlement européen sur l'intelligence artificielle, dit Artificial Intelligence Act (AI Act), qui vient d'être adopté par le Conseil et le Parlement européen. Un système d'IA, je cite, est « un système basé sur une machine, qui est conçu pour fonctionner avec différents niveaux d'autonomie et qui peut faire preuve d'adaptabilité après son déploiement et qui, pour des objectifs explicites ou implicites, déduit, à partir des données qu'il reçoit, comment générer des résultats tels que des prédictions, du contenu, des recommandations ou des décisions qui peuvent influencer des environnements physiques ou virtuels ». Trois mots sont importants dans cette définition : autonomie, données et résultats. Un système d'IA se nourrit de données, doit fonctionner de manière autonome et vise à produire un résultat comme attribuer un score ou proposer un choix entre oui et non.
L'IA existe depuis de nombreuses années et les systèmes experts bien programmés, qui ne sont pas autre chose que la résolution d'équations par ordinateur, ont déjà été utilisés dans le domaine de la santé. L'irruption de l'IA générative fonctionnant par auto-apprentissage ouvre toutefois de nouvelles perspectives en augmentant l'autonomie des systèmes capables d'apprendre par eux-mêmes à partir d'un très grand volume de données et d'enrichir les résultats. Il faut cependant garder à l'esprit les grandes différences entre les différentes catégories de systèmes d'IA, comme nous le faisaient remarquer les professeurs Brigitte Seroussi, Guillaume Assié ou encore le docteur Hernandez et le professeur Senhadji lors de leurs auditions, il y a une tension entre performance et explicabilité des différents modèles d'IA.
Ainsi, l'IA symbolique classique est très explicable mais a des performances limitées. Elle ne produit que ce pour quoi elle a été programmée, tandis que l'IA connexionniste, à la base de l'IA générative, qui fonctionne par rapprochements statistiques, est très performante, capable de donner des résultats que l'on n'avait pas prévus, mais est moins bien explicable.
Pour autant, l'IA générative pourrait être utilisée avec réussite dans le domaine de la santé, par exemple, pour mettre en forme des informations désordonnées ou pour produire des comptes rendus. L'Académie nationale de médecine a rendu récemment un rapport sur l'IA générative qui estime que son déploiement pourrait avoir un impact positif pour aider les médecins dans leurs pratiques quotidiennes.
Nous ne prétendons pas faire un panorama exhaustif de l'ensemble des utilisations de l'IA en santé, mais nous avons collecté de nombreux exemples qui permettent d'affirmer que son domaine d'application actuel et dans un futur proche, couvre un large spectre. En premier lieu, l'IA constitue un formidable accélérateur de recherche médicale. Je laisserai mon collègue Christian Redon-Sarrazy vous en dire plus sur ce sujet-là.
Un des domaines majeurs dans lesquels l'IA présente un grand intérêt est celui de l'imagerie médicale. Une étude américaine datant déjà de 2012 avait montré la grande performance des systèmes à base de réseaux convolutifs profonds pour lire les clichés radiologiques numérisés, faisant même dire à Geoffrey Hinton, spécialiste américain du deep learning, qu'il fallait arrêter de former des radiologues qui seraient rapidement dépassés par la machine. En réalité, ce remplacement du médecin par l'algorithme ne s'est pas produit, mais le métier de radiologue évolue rapidement. Des tâches de vérification ou de tri peuvent ainsi être automatisées avec un haut degré de fiabilité.
L'IA irrigue en vérité un très grand nombre de spécialités médicales. Pas moins de 700 dispositifs numériques médicaux intégrant l'IA ont fait l'objet d'une validation par la FDA (U.S. Food and Drug Administration) ou d'un marquage CE en Europe. On utilise l'IA en cancérologie pour identifier les tumeurs, leur stade de développement, affiner les pronostics, mais aussi assurer le suivi du traitement des patients. L'Institut national du cancer, que nous avons auditionné, estime qu'il existe aujourd'hui un potentiel énorme de l'IA en cancérologie. On utilise aussi l'IA en anatomopathologie pour lire les lames de pièces anatomiques. On l'utilise aussi en cardiologie, en neurologie, en néphrologie pour analyser la bonne adéquation entre greffon et greffé, comme nous l'a indiqué le professeur Alexandre Loupy.
Aussi, nous pouvons affirmer que l'intelligence artificielle en santé n'est pas un gadget, mais un outil supplémentaire capable d'apporter beaucoup à plusieurs niveaux. Les avantages de l'IA en santé sont en effet multiples.
Premier intérêt, elle peut améliorer la qualité des soins. En limitant les erreurs, en réduisant les pertes d'informations, en corrigeant les failles de prise en charge, par exemple en repérant les interactions médicamenteuses, l'IA pourrait ainsi harmoniser la qualité des soins par le haut et réduire les inégalités de prise en charge. Deuxième intérêt : faire gagner du temps en confiant à l'IA toute une série de tâches répétitives, les tâches administratives de collecte et d'enregistrement de données qui représentent une part importante du temps de travail des soignants. Certaines études parlent même de 25 % du temps des infirmières qui pourraient ainsi être gagné. Une étude de l'OCDE estime que l'IA pourrait automatiser plus d'un tiers de l'activité des services de santé et services sociaux. À l'APHP, un logiciel intégrant de l'IA guide les utilisateurs du dossier médical informatisé. Il repère les erreurs, émet des alertes, répond aussi aux questions des soignants. Troisième intérêt : l'IA pourrait contribuer à mieux organiser notre système de santé en réduisant les examens redondants ou encore en organisant mieux les blocs opératoires ou en aidant à mieux orienter les patients aux urgences. L'IA permet aussi d'anticiper les flux. À l'hôpital de Valenciennes, on ajuste les effectifs aux flux de patients attendus, estimés par une intelligence artificielle.
Un point suscite un espoir : l'IA pourrait aider à lutter contre les déserts médicaux. En rendant plus performante la télémédecine, nous pourrions organiser un service de santé de qualité dans les territoires ruraux ou périurbains où nous manquons cruellement de médecins. Certains examens pourraient être réalisés à distance ainsi que le suivi des patients, à condition toutefois que la couverture numérique du territoire soit satisfaisante et qu'une offre de télémédecine soit effectivement proposée localement. Soyons cependant mesurés sur ce sujet, l'IA ne résoudra pas le problème des déserts médicaux en installant des médecins numériques bourrés d'algorithmes pour soigner la population. Il sera toujours nécessaire d'avoir des intervenants humains capables d'échanger avec le patient, de coordonner sa prise en charge. C'est pourquoi nous devons veiller à une répartition plus équilibrée des moyens médicaux et paramédicaux sur l'ensemble du territoire.
L'IA pourrait au final conduire à une modification assez profonde de l'approche du soin. Notre médecine est aujourd'hui principalement curative. Or, la combinaison, d'une part, des avancées de la génomique, d'autre part, des données massives affine l'analyse que l'on peut faire de la santé actuelle et future de chaque individu. Nous pouvons ainsi basculer progressivement vers une médecine prédictive extrêmement personnalisée.
C'est un progrès si l'on parvient, en modifiant les comportements alimentaires ou autres, à prévenir des maladies futures. Mais le revers de la médaille réside dans le risque de faire du surdiagnostic et de s'attaquer inutilement à un large spectre de maladies futures possibles, mais pas du tout certaines, en créant d'autres problèmes : la surmédication, l'augmentation des dépenses d'examen de santé, du stress, etc.
La personnalisation à l'extrême de la médecine pourrait conduire à réinterroger à terme notre modèle d'assurance sociale. L'assurance maladie repose en effet sur la mutualisation du risque lié à la santé. Si la médecine prédictive permettait d'identifier les risques de dégradation de l'état de santé de chacun, de chiffrer les soins à recevoir individuellement, il existe un réel risque éthique de différencier soit les soins, soit leurs tarifications, les plus hauts profils de risques pouvant avoir du mal à s'assurer dans des conditions correctes.
Cependant, l'utilisation de l'IA est encore loin d'avoir atteint un rythme de croisière. Nous n'en sommes qu'au début et les illustrations que l'on a mises en avant ne sont pas encore généralisées. Même en imagerie médicale, l'IA est très développée mais n'a pas remplacé le radiologue. Elle le complète. En anatomopathologie, l'IA peut aider, mais l'absence de numérisation totale des lames empêche d'utiliser l'IA en routine.
Dans le secteur de la santé comme dans d'autres secteurs, l'IA est encore en phase d'apprentissage, avec un foisonnement d'initiatives autour d'équipes médicales motivées et d'entreprises innovantes. De ce bouillonnement pourraient naître des innovations majeures, mais gare aux déceptions. Car les conditions de réussite de l'IA en santé sont assez exigeantes, ce que nous allons voir dans la deuxième partie de cette présentation.
M. Christian Redon-Sarrazy, rapporteur. - Pour que l'IA apporte une réelle plus-value à notre système de santé, plusieurs éléments doivent en effet être réunis. Nous les avons regroupés sous trois grandes catégories. Il faut d'abord avoir accès à des données nombreuses et fiables. Ensuite, il nous faut poser un cadre éthique, car nous ne saurions confier notre santé à des robots autonomes et au fonctionnement opaque. Enfin, il faut un écosystème de l'action publique qui permette effectivement de tirer profit des technologies de l'IA, mais en n'étant pas totalement dépendant d'acteurs extérieurs. J'ajoute qu'il faut lever les réticences et les difficultés dans l'utilisation des outils de l'IA par les professionnels, en améliorant notamment la formation et en offrant les possibilités d'une acculturation, tant du côté des soignants que du côté des usagers du service public de la santé.
Avant d'aborder ces conditions de réussite de l'IA en santé, je souhaite revenir sur l'importance de l'IA aujourd'hui dans la recherche médicale. En effet, grâce à elle, on peut cribler des molécules-cibles, prédire l'activité médicamenteuse d'une molécule, modéliser en 3D des protéines, ce qui est important, par exemple, dans le domaine de la vaccination, et l'on sort d'une période où on en sait quelque chose.
L'IA aide aussi à réaliser des essais cliniques. On peut réduire la taille des groupes de contrôle. On peut constituer des jumeaux numériques pour simuler une opération. L'IA est bien ainsi un accélérateur de recherche qui permet d'effectuer très rapidement des synthèses, de procéder à des rapprochements de données, mais qui permet aussi, et surtout peut-être, d'ouvrir de nouvelles pistes.
Donc, en santé comme dans les autres domaines, pour que l'IA soit performante, encore, faut-il disposer de la matière première. Et aujourd'hui, la matière première, ce sont ces très nombreuses données qui sont stockées un peu partout. Si la puissance de calcul est bien le moteur de l'IA, la donnée en elle-même en est le carburant et l'accès à ces données est un enjeu stratégique pour les start-up et pour les équipes de recherche, les équipes médicales qui travaillent autour de l'IA. Le rapport Marchand-Arvier, qui a été remis fin 2023 et qui portait sur les données de santé, a, de l'avis de tous les acteurs que nous avons auditionnés, posé le bon diagnostic et formulé les bonnes propositions. La France, on le sait, dispose de très nombreuses données : feuilles de soins de la sécurité sociale, données des systèmes d'information des hôpitaux, cohortes de malades, d'essais cliniques, entrepôts de données de santé des hôpitaux.
Donc, la donnée, elle foisonne. Mais l'utilisation secondaire de ces données, c'est-à-dire leur utilisation hors d'une finalité directe de soin pour la personne concernée par ces données, notamment celle qui serait destinée à construire des algorithmes de diagnostic ou de traitement, se heurte à de nombreux freins dont le rapport Marchand-Arvier, a fait l'inventaire.
Le premier frein réside dans le caractère très éparpillé et très hétérogène des bases de données qui, de fait, ne les rend pas facilement utilisables. Le deuxième frein est dû à la durée et à la complexité des procédures réglementaires d'accès à ces données. C'est un sujet dont on entend régulièrement parler. Certes, la Cnil a établi des référentiels simplifiés, au nombre de 13, qui permettent un accès aux données sur simple déclaration dans 72 % des cas. Mais on sait bien que pour autant, il y a encore des opérateurs qui trouvent que c'est trop complexe et qu'il n'y a pas cette facilité qu'on pourrait avoir dans d'autres pays. On pourra en rediscuter. Lorsqu'on ne peut pas recourir à la déclaration, la procédure s'inscrit dans des délais courts : un mois pour l'avis d'un comité éthique et scientifique dénommé le Cesrees et deux mois pour l'avis de la Cnil. Mais le processus n'est pas facile à comprendre et à suivre pour des équipes de recherche qui parfois sont centrées sur d'autres objectifs que ces préoccupations d'ordre administratif.
Un troisième frein repose sur certaines difficultés de négociation entre les producteurs de données, qui sont par exemple les hôpitaux, et les producteurs d'algorithmes qui, eux, ont besoin de ces données. Les discussions sur les conditions financières de mise à disposition sont souvent longues, traînent et sont délicates, et n'aboutissent pas systématiquement. Au final, le délai moyen d'accès effectif aux données pour un projet de recherche est de l'ordre de 18 mois en France, ce qui est beaucoup plus qu'en Asie, par exemple, ou aux États-Unis. La France, en 2019, s'est dotée d'un outil pour faciliter l'accès aux données de santé, le fameux Health Data Hub, qui a pu accompagner plus de 100 projets et gère une plateforme technologique sécurisée.
Mais la confiance dans ce Health Data Hub, qui nous promettait peut-être à la fois de la souveraineté et de la facilité d'accès, a été fragilisée quand on nous a annoncé que les données étaient hébergées par Azure, une filiale de Microsoft, dans l'attente d'un cloud souverain sécurisé à l'horizon 2025. On est dans un domaine où les choses vont très vite. 2025, c'est 12 mois, mais pour les données, pour tous ceux qui opèrent dans ce secteur, c'est beaucoup.
Au-delà du seul enjeu de l'accès aux données, les fournisseurs de solutions d'intelligence artificielle attendent que ces données soient fiables et doivent faire les efforts pour lutter contre les biais, à condition de les repérer. Ces biais peuvent résulter d'un manque de représentativité des données d'entraînement. Ainsi, des différences de qualité de diagnostic en imagerie médicale avaient été constatées entre les hommes et les femmes. Il existe six sources de biais liés aux données numériques, aux essais cliniques antérieurs, à l'insuffisance de données dans certains domaines, aux préjugés cliniques (l'homme est passé par là avant), des biais de référence, des biais liés au profil de risque et des biais liés aux machines et aux algorithmes eux-mêmes. Ces multiples biais peuvent parfois se combiner et avoir des effets exponentiels. La plupart d'entre eux sont involontaires, mais les IA peuvent aussi, dans certains cas, être trompées par des données qui peuvent être volontairement falsifiées pour atteindre tel ou tel objectif.
Pour lutter contre l'ensemble de ces biais, ou tout au moins pour en limiter les effets, les systèmes d'IA doivent développer des filtres et faire des contrôles de cohérence. Donc, ils ne peuvent pas travailler de manière complètement non supervisée. En santé, plus encore que dans d'autres domaines, les systèmes d'IA doivent nécessairement faire l'objet d'un niveau de contrôle élevé. Les applications santé sont d'ailleurs situées au plus haut niveau de risque dans la classification de l'AI Act européen.
L'objectif est d'avoir une IA performante et donc d'abord de la nourrir correctement avec des données de santé qui soient à la fois nombreuses et de qualité. Mais une autre condition de réussite de l'IA en santé ne doit pas être oubliée : c'est bien sûr le fait que l'IA doive répondre à un cadre éthique solide. L'éthique, et je pense qu'on sera tous d'accord là-dessus, est indissociable de la pratique médicale. Ses principes ont été énoncés par les textes internationaux, qu'il s'agisse du code de Nuremberg, de la déclaration d'Helsinki, de la Convention d'Oviedo, et ils ont été déclinés au niveau national par les recommandations du Comité consultatif national d'éthique (CCNE). L'importance prise par le numérique en santé et par l'IA, dans un passé récent, ont donné lieu à la rédaction de lignes directrices de l'Organisation mondiale de la santé (OMS) et à l'échelle nationale, la formulation d'avis par le Comité national pilote d'éthique du numérique, une émanation du CCNE.
Les IA ne répondent en effet pas à des impératifs moraux. Ce sont des outils qui sont dotés d'une certaine autonomie de fonctionnement, mais bien sûr sans conscience et sans affect. Il est donc nécessaire d'encadrer ces outils pour éviter qu'ils ne soient manipulés ou utilisés à mauvais escient. Plusieurs principes éthiques s'imposent donc pour une utilisation vertueuse de l'IA en santé. Un des premiers, peut-être le plus important, c'est de protéger l'autonomie de la décision médicale. La décision ne doit pas totalement être déléguée à la machine. Le corollaire de cela, c'est le maintien d'une responsabilité humaine dans la mise en oeuvre de l'intelligence artificielle. D'ailleurs, je pense qu'on est tous plus enclins à accepter que l'homme se trompe plutôt que la machine. On sera beaucoup moins indulgent, peut-être, avec la machine, si elle seule devait nous fournir des diagnostics.
Le deuxième principe, c'est promouvoir le bien-être et la sécurité des personnes et l'intérêt public. L'IA ne doit pas être utilisée pour nuire. Le troisième principe est qu'il faut garantir une certaine transparence, une explicabilité et une intelligibilité de l'IA qui ne doit pas être une boîte noire incompréhensible. Patients comme médecins doivent être conscients de l'utilisation de l'IA et conscients aussi de ses limites. Cela rend nécessaire qu'il y ait toujours un contrôle humain in fine, que ce ne soit pas l'IA qui ait le dernier mot sur un diagnostic ou une décision.
Le quatrième principe est la garantie de l'inclusion et l'équité. Les IA ne doivent pas être discriminatoires. Il faut ensuite, cinquième principe, promouvoir une IA réactive et durable, notamment sur le plan environnemental. Quand on sait que l'un des principaux enjeux de l'IA, ce sont les données et quand on sait l'impact environnemental de tous ces entrepôts de données, cela interroge. Enfin, bien sûr, c'est le sixième principe, l'IA doit préserver la vie privée. La collecte de données ne peut pas s'accompagner d'une divulgation des informations personnelles de santé.
Après l'accès aux données et le cadre éthique, une troisième condition de réussite de l'IA en santé réside dans le soutien qu'elle aura ou qu'elle a déjà des pouvoirs publics. Le rapport Villani de 2018 avait donné un coup d'accélérateur. La Commission de l'intelligence artificielle, présidée par Philippe Aghion et Anne Bouverot, qui étaient venus présenter leur rapport devant notre délégation au cours d'une audition particulièrement intéressante, réclame 5 milliards d'euros d'investissement sur 5 ans et fait de la santé l'un des axes forts du développement de l'IA en France.
L'Agence de l'innovation en santé estime que l'on a déjà investi environ 400 millions d'euros d'argent public dans l'IA en santé à travers plusieurs dispositifs comme le PEPR Santé numérique. Il est clair qu'une stratégie d'accélération de l'IA en santé passe nécessairement par des soutiens publics forts.
Avant d'en venir à nos quatre axes de recommandations, je voudrais dessiner deux scénarios possibles pour l'IA en santé, l'un redouté, l'autre souhaité.
Le scénario redouté est celui du robot-médecin. Certes, il est évident que les systèmes d'IA n'ont pas aujourd'hui la capacité d'assurer une analyse complète du patient. Ils interviennent, souvent de manière très performante, pour répondre à une question précise comme la localisation de tumeurs, l'identification des biomarqueurs pertinents, la mise en forme d'informations médicales. Mais l'expérience des performances de l'IA peut conduire à une automatisation de nombreuses tâches d'analyse complexes, contribuant à déplacer l'expertise vers la machine. Dès lors, il existe un risque de déqualification dans le match entre l'homme et la machine. On risque de rater des cas complexes, nouveaux, non répertoriés. Faute de contrôle, on pourrait laisser passer des absurdités, les fameuses hallucinations de la machine. Cette menace est loin d'être immédiate, mais il faut en avoir une idée pour préférer un autre scénario bien plus vertueux.
Le bon scénario, à notre sens, est en effet celui du soignant augmenté. Comme le stéthoscope, comme l'électrocardiogramme, comme la radiologie - on parle de choses du siècle dernier, voire plus anciennes - l'IA constitue un outil supplémentaire pour les médecins et les équipes soignantes. Elle donne la possibilité de mieux connaître, de mieux comprendre le fonctionnement de nos organes et la manière de faire face à leur dysfonctionnement. Le professeur Loupy qualifiait l'IA de cognoscope, capable de rassembler des connaissances sur un patient, sur un mécanisme biologique et d'en tirer des recommandations. L'IA permettrait ainsi d'accélérer les prises en charge, de dépister et d'intervenir plus vite, d'affiner les diagnostics. Elle pourrait être une aide lorsque les ressources médicales et paramédicales font défaut. En ce sens, je rejoins ce qui a été dit sur les déserts médicaux. Des cabines de télémédecine connectées peuvent apporter sinon une solution, du moins un palliatif, à l'absence de médecin sur place.
Loin d'un techno-pessimisme qui est souvent de mise dans les débats publics, nous appelons à voir l'IA comme un outil de progrès sans céder à l'inverse au techno-enthousiasme béat, qui résulterait de stratégies de marketing bien rodées dont certaines firmes survendent les apports à notre société.
J'en viens maintenant aux quatre axes que nous avons identifiés pour une IA en santé efficace et juste : le premier, c'est développer une culture de l'IA en santé par la formation initiale et continue des soignants ; le deuxième, c'est accélérer l'accès des chercheurs et start-up aux données secondaires de santé ; le troisième est construire un cadre éthique robuste de l'IA en santé ; le quatrième vise à être capable de financer la course à l'IA.
Mme Anne Ventalon, rapporteure. - Le premier axe que nous avons identifié est donc développer une culture de l'IA en santé par la formation initiale et continue des soignants. Lors des auditions, on a vraiment entendu une unanimité sur le sujet. La formation est indispensable. Comme pour toute nouvelle technologie, son bon usage, voire son usage tout court, passe par une étape de prise en main par ses utilisateurs et ses bénéficiaires. Si l'informatique contemporaine se caractérise par d'importants efforts de fluidité et le souci du caractère très intuitif des interfaces hommes-machines, le fonctionnement de l'IA dans la santé doit être bien compris afin d'en tirer profit, mais aussi afin d'en mesurer les limites. La formation à l'intelligence artificielle devrait donc être intégrée au cursus universitaire pour les médecins, mais aussi les professions paramédicales. Pour adapter les personnels de santé déjà en poste, des efforts renforcés de formation continue à l'utilisation des outils d'IA devraient aussi être envisagés. Enfin, un nouveau métier d'opérateur de l'IA en santé pourrait voir le jour pour gérer la complexité et assurer une médiation entre les différents acteurs du système de santé, soignants, patients et producteurs de dispositifs médicaux numériques.
Le deuxième axe consiste à accélérer l'accès des chercheurs et start-up aux données secondaires de santé. L'accès aux données est une condition indispensable pour pouvoir développer des solutions de haut niveau fondées sur l'utilisation de l'intelligence artificielle. Cela est possible sans remise en cause fondamentale des grands principes de protection des données personnelles, en développant les méthodologies de référence (MR) dont le respect permet de se passer des procédures d'autorisation plus lourdes. Une part importante des délais d'accès ne résulte pas de verrous juridiques, mais de contraintes techniques. Il convient de faire adopter par le plus grand nombre de producteurs de données de santé des normes d'interopérabilité facilitant les croisements et de renforcer le rôle du Health Data Hub comme fédérateur des différentes bases de données. Enfin, des contrats types pourraient lever les verrous contractuels entre producteurs et utilisateurs de données, en définissant des normes de partage de la valeur.
M. Christian Redon-Sarrazy, rapporteur. - Le troisième axe est construire un cadre éthique robuste de l'IA en santé. La confiance dans l'IA de la part de l'ensemble des acteurs de la santé, patients comme professionnels, est conditionnée au respect des principes éthiques garantissant le caractère fiable et non discriminant du fonctionnement des IA mises à disposition pour notre santé, la protection des données personnelles de santé qui sont des données sensibles que l'on ne souhaite pas voir être exposées sur la place publique ou encore l'absence de délégation complète de la prise de décisions importantes à la machine. Patients comme soignants doivent pouvoir comprendre avec précision la portée et les limites de l'utilisation des solutions d'IA disponibles.
Les exigences éthiques doivent être intégrées dans les dispositifs d'IA dès leur conception. L'expression anglaise, c'est Ethics by design. Et les enjeux d'éthique doivent être intégrés eux aussi dans la formation des soignants à l'IA. Enfin, les exigences éthiques doivent trouver leur traduction juridique dans les textes et leur mise en application concrète. Le caractère dissuasif des sanctions prévues par l'AI Act européen, en cas de manquement des fournisseurs de services numériques à risque élevé à leurs obligations, c'est une amende de 35 millions d'euros ou de 7 % du chiffre d'affaires, ce qui constitue une forte incitation à placer la barre haut en matière d'éthique. Il conviendra toutefois que les instances nationales le contrôlent, en France avec la Cnil qui dispose de moyens renforcés d'investigation et d'expertise pour que la menace de sanction puisse jouer à plein.
Le dernier axe, c'est celui des moyens, c'est être capable de financer la course à l'IA. Dans le domaine de la santé comme dans les autres domaines, l'IA connaît un essor qui se traduit par la multiplication d'initiatives et d'expérimentations, parfois en ordre très dispersé. L'irruption de l'IA générative a donné un coup d'accélérateur aux investissements et contribue à faire évoluer très vite les technologies et leurs possibilités d'application. Cette phase expérimentale un peu foisonnante qui repose sur une multitude d'acteurs plus ou moins structurés, pourrait être suivie d'une phase de stabilisation qui ne laissera que quelques opérateurs sur le marché. Le rapport de la Commission de l'intelligence artificielle de mars 2024 alerte sur le risque de rater la marche et de dépendre in fine de firmes américaines ou chinoises. L'ambition d'un écosystème de l'IA en santé, peu dépendant de partenaires étrangers, passe par un investissement public demandé par la Commission de l'IA, mais aussi par l'accélération du projet de cloud sécurisé souverain, car nos données de santé, au même titre que nos données de sécurité ou nos données fiscales, ne sauraient être soumises au risque de transmission à une puissance étrangère.
Enfin, la course à l'IA ne trouvera un aboutissement concret pour les patients que si, au-delà des investissements initiaux, un modèle économique est trouvé pour financer les nouveaux outils par une tarification adaptée. Il s'agit là d'un sacré défi. Il s'agit de disposer de fonds au-delà de la seule phase de mise en route et de ce point de vue, une enveloppe dédiée au secteur hospitalier pourrait, sur le modèle du financement des missions d'intérêt général, favoriser l'acquisition et la maintenance de solutions logicielles performantes.
Merci pour votre attention sur un sujet complexe qui nous a passionnés. Comme vous le souhaitiez, madame la présidente, le document que nous vous présentons est assez ramassé mais complet malgré tout et je crois qu'il balaie un peu tous les enjeux.
Mme Anne Ventalon, rapporteure. - Je m'associe à ces propos. Avec ce sujet, nous sommes tous les deux sortis de notre zone de confort. C'est un beau défi parce qu'effectivement le sujet est complexe, mais il nous a permis d'avoir des échanges passionnants et de rencontrer des gens passionnés. Il est vrai que pour faire accepter l'intelligence artificielle, il faut la faire comprendre et savoir être didactique. C'est ce que nous avons tenté de faire avec ce rapport.
Mme Christine Lavarde, présidente. - Merci à vous deux. Effectivement, le cahier des charges est parfaitement rempli. Après vous avoir écoutés, notamment sur la façon dont l'IA pourrait permettre de lutter contre les déserts médicaux, j'ai compris que vous étiez plus en faveur du soignant augmenté que du robot médecin. Mais pour avoir expérimenté une fois la téléconsultation en cabine dans une pharmacie, j'ai eu le sentiment que si j'avais eu un robot médecin face à moi, j'aurais peut-être été mieux auscultée que par ce médecin en vidéo. Pour ce cas de figure assez précis des cabines de téléconsultation, on se situe quand même dans un environnement médical puisqu'elles sont installées dans des pharmacies où l'on a des professionnels capables d'analyser l'ordonnance qui sera émise après la téléconsultation. Est-ce que dans ce cas, on ne pourrait pas avoir des robots médecins ? Parce que finalement, quand on nous dit : « ouvrez grand la bouche, mettez ça dans l'oreille, mettez ça sur votre front... », c'est une donnée qu'on envoie et le robot serait, à mon avis, tout aussi capable de l'analyser que le médecin qui est de l'autre côté de la caméra. Cet exemple permet peut-être d'apporter une petite nuance à vos propos.
M. Jean-Jacques Michau. - C'est extrêmement intéressant. Vous avez parlé de souveraineté et d'investissement et aussi des États-Unis et de la Chine. Est-ce que le niveau national est suffisant pour investir dans l'IA ou est-ce qu'un niveau européen permettrait de disposer de davantage de moyens ? En écho à vos propos sur les territoires, l'intelligence artificielle sera-t-elle plutôt un réducteur d'inégalités ou au contraire, l'occasion d'accroître la santé à plusieurs vitesses ?
Mme Marie-Pierre Richer. - Merci pour ce rapport et d'avoir mis à notre portée ce sujet complexe. Vous parlez d'un métier d'opérateur en IA : avez-vous identifié des formations ? Sur combien d'années se feraient-elles ? Est-ce que ce métier existe déjà ailleurs qu'en France ? Ensuite, j'ai noté un délai moyen d'accès aux données de santé de 18 mois, plus long qu'aux USA et en Asie. Quel est-il dans ces pays ? Enfin, on parle beaucoup de logiciels d'IA, je pense notamment à la cancérologie et plus particulièrement au cancer du sein, où l'on sait que l'IA a permis des progrès considérables et des gains de temps pour les oncologues. Est-ce que cette technique est développée sur l'ensemble du territoire ? À quelle vitesse se développe-t-elle ? Je suppose qu'il y a des centres beaucoup plus avancés que d'autres.
Mme Patricia Demas. - Merci à nos deux rapporteurs qui nous permettent d'avoir accès à des sujets assez complexes. J'ai deux questions. La première relève de la sécurité des données et de la cybersécurité en matière d'IA : y a-t-il des garde-fous ? La seconde : est-il possible de contrarier un diagnostic de l'IA et à quel moment ? Est-ce bien prévu ?
M. Stéphane Sautarel. - Merci également pour le travail accompli. Il me semble qu'il se passe beaucoup de choses aux États-Unis, qui est sans doute le pays le plus en pointe sur le sujet. J'ai lu récemment que les diagnostics médicaux via l'IA y étaient opérationnels et très développés. Qu'en est-il dans notre pays ? J'ai une interrogation sur les domaines d'application de l'IA. Les statistiques de France Biotech que vous présentez dans le rapport semblent montrer qu'il y a des baisses dans certains domaines. Est-ce qu'il s'agit d'une baisse relative par rapport à l'ensemble des domaines ? Je pensais que tout était à la hausse et je suis surpris de voir que sur des sujets, uniquement de données type dossier médical, ou outils destinés aux payeurs, on n'était pas plus avancé, alors que cela pose moins de questions éthiques que d'autres sujets.
Mme Annick Jacquemet. - Merci chers collègues pour votre rapport et les explications très claires que vous nous avez fournies. Vous avez parlé de la redondance des soins. On évoque couramment un tiers de soins redondants, avec bien sûr les coûts de sécurité sociale qui vont avec. En quoi l'intelligence artificielle pourrait-elle intervenir et comment pourrait-elle intervenir ? La prescription étant le fait des médecins, quel est le lien possible ?
Mme Anne Ventalon, rapporteure. - Je commencerai par répondre à la question sur la lutte contre les déserts médicaux. Vous avez compris nos conclusions, la situation actuelle n'est pas satisfaisante. Développer la téléconsultation est une option même si, pour l'instant, les consultations restent dans le domaine du non-complexe, par exemple pour le renouvellement d'une ordonnance ou pour obtenir un diagnostic. Sur le médecin robot, on nous a même dit qu'il pouvait développer une empathie plus grande que certains humains. Cela nous a fait sourire mais nous avons retenu ce paramètre. En tout état de cause, on peut y recourir pour des activités simples. Pour des recherches ou des auscultations plus approfondies, le médecin robot n'est pas satisfaisant.
M. Christian Redon-Sarrazy, rapporteur. - Ce qui a été souligné parfois aussi, c'est le gain de temps. L'IA peut aussi, pour des consultations de base, permettre de dégager du temps pour le médecin. Après, quid de l'utilisation de ce temps dégagé ? Comment l'utilise-t-on pour une meilleure couverture médicale ? Il y a une première phase pendant laquelle l'IA peut procurer des gains, mais ensuite il faut que la communauté soit prête à les utiliser de manière mutualisée.
Mme Anne Ventalon, rapporteure. - Le gain de temps, c'est pour gagner en qualité de soins et permettre aux médecins d'avoir une approche plus humaine dans l'accompagnement des patients. À la question « peut-on contrarier le diagnostic ? », même aux États-Unis, l'IA relève encore de l'ordre de l'expérimentation. L'IA est un outil qui vient aider et accompagner le diagnostic.
M. Christian Redon-Sarrazy, rapporteur. - Les investissements qui pourraient être faits dans l'IA sont de plusieurs ordres. Dans le secteur de l'hôpital, il n'y a pas de pilotage national de projets d'IA. Certains groupements hospitaliers de territoire avancent plus ou moins vite. Ensuite, il y a les investissements dans les start-up qui émergent, les projets de recherche qui ont besoin d'être soutenus et qui pourraient nous donner des solutions un peu plus souveraines. On est confronté aujourd'hui à des systèmes d'IA entraînés sur des données de santé américaines parce que les applications sont développées aux États-Unis, donc sur des populations qui n'ont pas nécessairement les mêmes caractéristiques que les populations européennes. Mais dans tous les cas, l'échelle des investissements, c'est au moins l'échelle européenne, parce qu'on sait, dans l'IA comme dans tous les domaines de recherche, que la taille du marché français n'est pas suffisante. Il faut donc des plans de soutien massifs et coordonnés à l'échelle européenne.
Ce qui m'a marqué dans les auditions, c'est que l'on a des médecins très volontaristes, parfois très en avance, mais on a l'impression que certains avancent seuls. Le risque, c'est de voir se développer une certaine inégalité, pas nécessairement territoriale, mais liée à la performance d'un groupe de recherche, d'un CHU ou d'un écosystème autour de la santé. Il y a tout un travail de structuration à faire pour un déploiement massif de l'IA.
Mme Anne Ventalon, rapporteure. - La cybersécurité est un vrai sujet, c'est la condition essentielle pour avoir confiance en l'intelligence artificielle. L'audition avec le Health Data Hub a bien montré la nécessité de sécuriser au maximum les données, notamment dans les liens avec Microsoft. Et effectivement, on n'avancera pas tant qu'on n'aura pas la garantie d'avoir cette protection des données.
Sur le nouveau métier d'opérateur en IA, il est vrai qu'on a un discours de certains professionnels de santé qui craignent de se voir dépossédés de leur savoir médical. Mais il n'y a pas de de concurrence, c'est vraiment quelque chose qui doit venir en plus et qui reste à définir. Il y a toutefois cette volonté de former et de créer un nouveau métier pour coordonner toutes les données et les diffuser.
M. Christian Redon-Sarrazy, rapporteur. - Le besoin de formation est à tous les niveaux de la chaîne de soins, depuis le médecin généraliste qui va notamment orienter, jusqu'aux différentes spécialités ou procédures de soins qui, les unes après les autres, peuvent bénéficier de l'IA.
Le dossier médical partagé est essentiel et l'IA peut être très performante pour mieux l'alimenter avec, par exemple, l'analyse de comptes rendus divers et variés qui fera gagner du temps. Elle permettra aussi des gains financiers avec moins de doubles ou triples diagnostics et de prescriptions multiples. Mais cela nécessite une harmonisation des données et donc que les systèmes de données puissent se parler entre eux. L'IA peut avoir un rôle important dans sa capacité à croiser des données aujourd'hui entreposées dans des systèmes différents.
Une précision sur le délai d'accès aux données aux États-Unis, il peut être de quelques jours seulement, à comparer aux 18 mois évoqués pour la France.
M. Stéphane Sautarel. - J'observe que, dans le domaine de la santé, on retrouve une caractéristique qui avait été évoquée dans le rapport sur les services fiscaux et sociaux, c'est-à-dire l'importance des initiatives isolées, particulières, personnelles, par goût ou plutôt par absence de structuration ou de pilotage à une échelle plus globale.
M. Christian Redon-Sarrazy, rapporteur. - C'est un point de vigilance en effet. Nous avons d'ailleurs mentionné la nécessité d'une évaluation des différents outils. Une start-up avec un service marketing et commercial très pertinent peut proposer un outil a priori hyper intéressant, par exemple dans le domaine du dépistage du cancer du sein ou de l'interprétation des lames d'anatomopathologie. Pour le détourage des zones qui vont être traitées par radiothérapie, fait aujourd'hui manuellement par un médecin, l'IA serait très utile car elle permettrait précision quasi chirurgicale.
Il y a donc déjà de vraies avancées, mais encore faut-il qu'elles soient correctement réparties sur le territoire et que les réticences de certains professionnels soient levées.
Mme Anne Ventalon, rapporteure. - Au cours des auditions, nous avons bien senti l'écart entre ceux qui sont en avance et utilisent l'IA de manière efficace dans leur pratique quotidienne et ceux qui ont une attitude plus mesurée. Il est vrai aussi qu'ils ne font pas tous le même travail. Il y a une vraie diversité de situations.
Mme Marie-Pierre Richer. - Je connais une personne qui travaille sur des logiciels en lien avec le cancer du sein et qui se désolait que la France ne s'en empare pas plus rapidement alors que l'Allemagne, où elle est partie, lui semblait beaucoup moins rétive. Je pense à la perte de chance qu'il peut y avoir dans une telle situation car on gagne du temps en pouvant extrapoler la progression des cellules cancéreuses.
Mme Anne Ventalon, rapporteure. - On nous a aussi alertés sur ces fuites vers l'étranger.
Mme Christine Lavarde, présidente. - Approuvez-vous ce rapport et êtes-vous d'accord pour qu'il soit rendu public ?
La délégation adopte le rapport à l'unanimité et en autorise la publication.
Merci à nos rapporteurs auxquels je souhaite le même succès que pour le premier rapport de la délégation sur l'IA. Tous ceux qui l'ont lu en reparlent. Comme il est exactement dans la même veine, il devrait rencontrer lui aussi son public.
LISTE DES PERSONNES ENTENDUES
· Health Data Hub
Stéphanie Combes, directrice
Nicolas Bellière, chef de cabinet
· France Biotech
Franck Mouthon, président
Alexandre Regniault, vice-président
Olivier Chabanon, directeur général
Mathieu Bouthemy, responsable des relations institutionnelles et affaires publiques
Maximilien Levesque, directeur général de la société Aqemia
Sébastien Mourey, directeur général de la société Screen act
Olivier Vire, directeur général de la société Medipath
Mathieu Rimaud, directeur général de la société Twinsight
· Doctolib
Mélanie Lemeunier, directrice du département médico-légal
Camille Vaziaga, directrice des affaires publiques
Marie-Charlotte Dexmier
· Pr Guillaume Assié, endocrinologue à l'hôpital Cochin-Port Royal AP-HP, directeur de la chaire IA et santé, Université Paris cité
· Pr Brigitte Séroussi, professeure d'informatique biomédicale, Sorbonne Université
· Agence de l'innovation en santé
Lise Alter, directrice générale
Charles-Édouard Escurat, directeur Pôles Accélérations et Accompagnement
· Pr Jean-Emmanuel Bibault, auteur du livre 2041 : l'odyssée de la médecine, comment l'intelligence artificielle bouleverse la médecine
· Romain Bey, spécialiste de l'exploitation des données de santé
· Inserm
Dr Alexandre Loupy, néphrologue, lauréat du Prix Inserm Innovation 2023
Anne-Sophie Etzol, responsable des relations institutionnelles
· Assistance publique-Hôpitaux de Paris (AP-HP), Direction des services numériques (DSN)
Caroline Germain, directrice du pôle Innovation et données
Dr Christel Gérardin, médecin Interniste, PhD en informatique biomédicale
Vincent Rubod, responsable projets plateforme de données massives AP-HP
Perceval Wajsburt, PhD Senior Data scientist, responsable du développement NLP (traitement automatique du langage)
Thomas Petit-Jean, Senior Data scientist, directeur par intérim du service Data Science
Ariel Cohen, Senior Data scientist, Responsable du pôle analyse
Quentin Demanet, adjoint au directeur de la recherche clinique, de l'innovation et de la relation avec les universités
Dr Claire Hassen-Khodja, médecin de santé publique
· Fédération hospitalière de France (FHF)
Dr Frédéric Martineau, radiologue et conseiller médical
Laurent Pierre, conseiller numérique
· Conseil national de l'ordre des médecins
Pr Stéphane Oustric, conseiller national délégué général aux données de santé et au numérique
Lou Rodriguez, chef du service du droit du numérique
· Pr Bernard Nordlinger, président du Cesrees (Comité éthique et scientifique pour les recherches, les études et les évaluations en santé)
· McKinsey France
Thomas London, responsable du pôle Santé
· Institut national du cancer (INCa)
Pr Norbert Ifrah, président
Frédéric De Bels, responsable du département Prévention
Christine Le Bihan, responsable du département Données et évaluation en santé
· Laboratoire Traitement du signal et de l'image (LTSI). Inserm U1099. Rennes
Dr Alfredo Hernandez, directeur de recherche Inserm
Pr Lotfi Senhadji, professeur des universités à l'université de Rennes
* 1 Bernard Nordlinger, Claude Kirchner, Olivier de Fresnoye, Systèmes d'IA générative en santé : enjeux et perspectives, 5 mars 2024.
* 2 European Alliance for access to Safe Medicines, « Medication Errors - the Most Common Adverse Event in Hospitals Threatens Patient Safety and Causes 160,000 Deaths per Year », 13 septembre 2022 ; https://eaasm.eu/fr/2022/09/13/press-release-medication-errors-the-most-common-adverse-event-in-hospitals-threatens-patient-safety-and-causes-160000-deaths-per-year-4/.
* 3 Haute Autorité de santé, Évènements indésirables graves associés aux soins (EIGS) : bilan annuel 2022, novembre 2023 ; https://www.has-sante.fr/jcms/p_3472509/fr/evenements-indesirables-graves-associes-aux-soins-eigs-bilan-annuel-2022.
* 4 OCDE, L'IA dans le domaine de la santé, un immense potentiel, d'énormes risques, 2024 ; https://www.oecd.org/fr/sante/IA-en-sante-immense-potentiel-enormes-risques.pdf (consulté le 04/04/2024).
* 5 Drees, « Deux tiers des médecins généralistes libéraux déclarent travailler au moins 50 heures par semaine », Études et résultats, n° 1113, 7 mai 2019 ; https://drees.solidarites-sante.gouv.fr/publications/etudes-et-resultats/deux-tiers-des-medecins-generalistes-liberaux-declarent-travailler.
* 6 Étude de l'OCDE précitée.
* 7 France 3 Bretagne, « Santé, comment l'intelligence artificielle réduit le temps de prise en charge aux urgences du CHU de Rennes », 26 septembre 2023 ; https://france3-regions.francetvinfo.fr/bretagne/ille-et-vilaine/rennes/sante-comment-l-intelligence-articifielle-reduit-le-temps-de-prise-en-charge-aux-urgences-du-chu-de-rennes-2846378.html.
* 8 OCDE, rapport annuel, Health at a Glance 2023, 7 novembre 2023 ; https://www.oecd.org/health/health-at-a-glance/.
* 9 Le logiciel AlphaFold2, développé par DeepMind, filiale de Google.
* 10 Pour une revue de l'utilisation de technologies d'IA dans la crise du covid-19, voir l'article sur le site du Conseil de l'Europe, « IA et lutte contre le coronavirus Covid-19 » ; https://www.coe.int/fr/web/artificial-intelligence/ai-and-control-of-covid-19-coronavirus (consulté le 02/04/2024).
* 11 Pour en savoir plus, voir une analyse succincte du cabinet KPMG, « Intelligence artificielle et recherche clinique, la grande accélération » ; https://kpmg.com/fr/fr/home/kpmg-innovation-lab/exploration/intelligence-artificielle-et-recherche-clinique-la-grande-acceleration.html (consulté le 02/04/2024).
* 12 Un exemple : https://www.inc.cnrs.fr/fr/cnrsinfo/ia-et-candidats-medicaments-une-nouvelle-methode-de-conception-par-traitement-numerique.
* 13 Alex Krizhevsky, Ilya Sutskever, Geoffrey E. Hinton, « ImageNet Classification with Deep Convolutional Neural Networks », Advances in Neural Information Processing Systems 25 (NIPS 2012) ; https://papers.nips.cc/paper_files/paper/2012/hash/c399862d3b9d6b76c8436e924a68c45b-Abstract.html (consulté le 02/04/2024).
* 14 Léo Mignot, Émilien Schultz, « Les innovations d'intelligence artificielle en radiologie à l'épreuve des régulations du système de santé », Réseaux, 2022/2-3 (N° 232-233), p. 65-97. DOI : 10.3917/res.232.0065 ; URL : https://www.cairn.info/revue-reseaux-2022-2-page-65.htm (consulté le 02/04/2024).
* 15 Source : « Radiologie : pourquoi l'IA n'a (toujours) pas remplacé le médecin », theconversation.com, 28 juin 2022 https://theconversation.com/radiologie-pourquoi-lia-na-toujours-pas-remplace-le-medecin-185319 (consulté le 02/04/2024).
* 16 Voir notamment l'article sur le site de l'INRIA : « Imagerie médicale : l'intelligence artificielle peut-elle tenir ses promesses ? », www.inria.fr, 11 mai 2022 ; https://www.inria.fr/fr/imagerie-medicale-intelligence-artificielle-apprentissage-automatique (consulté le 02/04/2024).
* 17 Yan Chen, Adnan G. Taib, Iain T. Darker, Jonathan J. James, « Performance of a Breast Cancer Detection AI Algorithm Using the Personal Performance in Mammographic Screening Scheme », RSNA, 5 septembre 2023 ; https://pubs.rsna.org/doi/10.1148/radiol.223299.
* 18 Paolo Giorgi Rossi et al., « Comparing accuracy of tomosynthesis plus digital mammography or synthetic 2D mammography in breast cancer screening: baseline results of the MAITA RCT consortium », Eur J Cancer, mars 2024 ; https://pubmed.ncbi.nlm.nih.gov/38262307/.
* 19 HAS, Évaluation de la performance et de la place de la mammographie par tomosynthèse dans le programme national de dépistage organisé du cancer du sein - Volet 2, validé par le Collège le 9 février 2023, mis à jour en avril 2023 ; https://www.has-sante.fr/jcms/p_3148278/fr/evaluation-de-la-performance-et-de-la-place-de-la-mammographie-par-tomosynthese-dans-le-programme-national-de-depistage-organise-du-cancer-du-sein-volet-2.
* 20 Sifem, « Apport de l'intelligence artificielle dans le dépistage du cancer du sein », www.imageriedelafemme.org, 12 février 2024 ; https://www.imageriedelafemme.org/apport-de-lintelligence-artificielle-dans-le-depistage-du-cancer-du-sein/ (consulté le 02/04/2024).
* 21 « Dépistage du cancer du sein : l'intelligence artificielle doit trouver sa juste place », Le Monde, 4 avril 2024 ; https://www.lemonde.fr/sciences/article/2024/04/04/depistage-du-cancer-du-sein-l-intelligence-artificielle-doit-trouver-sa-juste-place_6225918_1650684.html.
* 22 Wu J, Gale CP, Hall M, et al., « Editor's Choice - Impact of initial hospital diagnosis on mortality for acute myocardial infarction: A national cohort study », European Heart Journal: Acute Cardiovascular Care, 2018;7(2):139-148 ; https://journals.sagepub.com/doi/abs/10.1177/2048872616661693?journalCode=acca.
* 23 Paris Institute for Transplantation & Organ Regeneration (PITOR).
* 24 Rapport du Comité international de bioéthique de l'Unesco (CIB) sur les aspects éthiques des neurotechnologies, 2023, Rev. Paris, 56p. [En ligne]. https://unesdoc.unesco.org/ark:/48223/pf0000378724_fre.
* 25 Mayo Clinic, Deep Brain Stimulation, 19 septembre 2023.
*
26 Sur cette question, consulter notamment la note
scientifique de l'Office parlementaire d'évaluation des choix
scientifiques et technologiques (OPECST) : Patrick Hetzel, Les
neurotechnologies : défis scientifiques et éthiques, 22
janvier 2022.
https://www.senat.fr/fileadmin/Office_et_delegations/OPECST/Notes_scientifiques/OPECST_note32.pdf.
* 27 Éthique des neurotechnologies, UNESCO, 2024. https://www.unesco.org/fr/ethics-neurotech.
* 28 Audition du Pr Raphaël Gaillard, chef du pôle hospitalo-universitaire de psychiatrie de l'hôpital Sainte-Anne, par la délégation à la prospective, le 21 mars 2024 ; https://www.senat.fr/compte-rendu-commissions/20240318/pro_2024_03_21.html.
* 29 Baromètre national réalisé par PulseLife et Interaction Healthcare sur l'impact de l'intelligence artificielle (IA) dans la pratique médicale, réalisé à partir de l'interrogation de 1 700 professionnels de santé, 1er février 2024 : https://pulselife.com/fr-fr/blog/post/barometre-ia-en-sante-alliee-ou-menace.
* 30 Healthcare Data Institute, HDI Day, Les Français, les professionnels de santé et l'intelligence artificielle, 29 novembre 2023 ; https://healthcaredatainstitute.com/2024/01/14/ia-en-sante-des-ecarts-de-perception-et-dusage-entre-francais-et-medecins-reveles-par-deux-etudes-du-healthcare-data-institute/.
* 31 Rapport n° 589 de M. Bruno Rejouan fait au nom de la commission de l'aménagement du territoire et du développement durable, Rétablir l'équité territoriale en matière d'accès aux soins : agir avant qu'il ne soit trop tard, déposé le 29 mars 2022 ; https://www.senat.fr/notice-rapport/2021/r21-589-notice.html.
* 32 Healthcare Data Institute, Jusqu'où les données peuvent-elles accompagner la transformation de la santé par l'IA ?, 26 mars 2024 ; https://healthcaredatainstitute.com/wp-content/uploads/2024/03/healthcare_data_institute_hdi_rapport_ia_sante_vf1.pdf.
* 33 Source : NIH ; https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6135136/.
* 34 Jérôme Marchand-Arvier, Fédérer les acteurs de l'écosystème pour libérer l'utilisation secondaire des données de santé, 1er décembre 2023 ; https://sante.gouv.fr/IMG/pdf/rapport_donnees_de_sante.pdf.
* 35 Voir l'étude américaine datant de 2020 : Larrazabal AJ, Nieto N, Peterson V, Milone DH, Ferrante E., « Gender imbalance in medical imaging datasets produces biased classifiers for computer-aided diagnosis », Proc Natl Acad Sci USA, 9 juin 2020 ; https://pubmed.ncbi.nlm.nih.gov/32457147/.
* 36 Voir l'étude américaine datant de 2024 : Perets O, Stagno E, Yehuda EB, McNichol M, Anthony Celi L, Rappoport N, Dorotic M., « Inherent Bias in Electronic Health Records: A Scoping Review of Sources of Bias », medRxiv [Preprint], 12 avril 2024 ; https://pubmed.ncbi.nlm.nih.gov/38680842/.
* 37 World Health Organization, Ethics and governance of artificial intelligence for health - WHO guidance, 28 juin 2021 ; https://www.who.int/publications/i/item/9789240029200.
* 38 World Health Organization, Ethics and governance of artificial intelligence for health: guidance on large multi-modal models, 2024 ; https://iris.who.int/handle/10665/375579.
* 39 Quatre avis rendus :
- n° 7 du 30 juin 2023 « Systèmes d'intelligence artificielle générative : enjeux d'éthique » ;
- n° 5 du 9 mai 2023 « Plateformes de données de santé : enjeux d'éthique » ;
- n° 4 du 10 janvier 2023 « Diagnostic médical et intelligence artificielle : enjeux éthiques » ;
- n° 3 du 9 novembre 2021 « Agents conversationnels : enjeux d'éthique ».
* 40 Philippe Aghion, Anne Bouverot, IA : notre ambition pour la France, 15 mars 2024 ; https://www.vie-publique.fr/rapport/293444-ia-notre-ambition-pour-la-france.
* 41 Audition de Philippe Aghion et Anne Bouverot, co-présidents de la Commission de l'intelligence artificielle, par la délégation à la prospective, le 26 mars 2024 ; https://www.senat.fr/compte-rendu-commissions/20240325/pro_2024_03_26.html.